Разрешительная документация на исследования мелких лабораторных животных. Общие методические и организационные подходы к проведению исследований и учебной практики по зоологии позвоночных
ГОСТ 33216-2014
Группа Т58
МЕЖГОСУДАРСТВЕННЫЙ СТАНДАРТ
РУКОВОДСТВО ПО СОДЕРЖАНИЮ И УХОДУ ЗА ЛАБОРАТОРНЫМИ ЖИВОТНЫМИ
Guidelines for accommodation and care of animals. Species-specific provisions for laboratory rodents and rabbits
МКС 13.020.01
Дата введения 2016-07-01
Предисловие
Цели, основные принципы и основной порядок проведения работ по межгосударственной стандартизации установлены в ГОСТ 1.0-92 "Межгосударственная система стандартизации. Основные положения" и ГОСТ 1.2-2009 "Межгосударственная система стандартизации. Стандарты межгосударственные, правила, рекомендации по межгосударственной стандартизации. Правила разработки, принятия, применения, обновления и отмены"
Сведения о стандарте
1 РАЗРАБОТАН Некоммерческим партнерством "Объединение специалистов по работе с лабораторными животными" (Rus-LASA)
2 ВНЕСЕН Техническим комитетом по стандартизации ТК 339 "Безопасность сырья, материалов и веществ"
3 ПРИНЯТ Межгосударственным советом по стандартизации, метрологии и сертификации (протокол от 22 декабря 2014 г. N 73-П)
Краткое наименование страны по | Сокращенное наименование национального органа по стандартизации |
|
Азербайджан | Азстандарт |
|
Беларусь | Госстандарт Республики Беларусь |
|
Казахстан | Госстандарт Республики Казахстан |
|
Киргизия | Кыргызстандарт |
|
Молдова | Молдова-Стандарт |
|
Россия | Росстандарт |
4 Приказом Федерального агентства по техническому регулированию и метрологии от 9 ноября 2015 г. N 1733-ст межгосударственный стандарт ГОСТ 33216-2014 введен в действие в качестве национального стандарта Российской Федерации с 1 июля 2016 г.
5 Настоящий стандарт соответствует международному документу European Convention for the protection of Vertebrate animals used for experimental and other scientific purposes (ETS N 123)* (Европейская конвенция о защите позвоночных животных, используемых в экспериментах и в других научных целях (ETS N 123)).
________________
* Доступ к международным и зарубежным документам, упомянутым здесь и далее по тексту, можно получить, перейдя по ссылке на сайт http://shop.cntd.ru . - Примечание изготовителя базы данных.
Перевод с английского языка (en).
Степень соответствия - неэквивалентная (NEQ)
6 ВВЕДЕН ВПЕРВЫЕ
Информация об изменениях к настоящему стандарту публикуется в ежегодном информационном указателе "Национальные стандарты", а текст изменений и поправок - в ежемесячном информационном указателе "Национальные стандарты". В случае пересмотра (замены) или отмены настоящего стандарта соответствующее уведомление будет опубликовано в ежемесячном информационном указателе "Национальные стандарты". Соответствующая информация, уведомление и тексты размещаются также в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет
Введение
Введение
Государства - члены Совета Европы приняли решение о том, что их целью является охрана животных, используемых для экспериментальных и других научных целей, которое является гарантией того, что возможные боль, страдание, дистресс или повреждения, имеющие длительные последствия для здоровья, возникающие в результате процедур, будут сведены к минимуму.
Результатом стало подписание и ратификация большинством государств - членов Совета Европы (все государства Евросоюза, а также Македония, Норвегия, Сербия, Соединенное Королевство Великобритании и Северной Ирландии, Швейцария) Конвенции об охране позвоночных животных, используемых для экспериментов или в других научных целях ETS N 123, Страсбург, 18 марта 1986 г. (далее Конвенция).
Конвенция распространяет свое действие на все виды деятельности, связанные с использованием лабораторных животных: размещение и уход за ними, проведение экспериментов, гуманное умерщвление (эвтаназия), выдача разрешений на использование животных в процедурах, контроль над заводчиками, поставщиками и пользователями, обучение и профессиональная подготовка кадров, статистический учет. Конвенция имеет два технических приложения, содержащих руководство по содержанию и уходу за лабораторными животными (приложение А) и таблицы для представления статистической информации о количестве животных, использованных в научных целях (приложение В).
Минимум один раз в пять лет Конвенция подлежит пересмотру в ходе многосторонних консультаций сторон, проводимых рабочей группой, с целью анализа соответствия ее положений меняющимся обстоятельствам и новым научным данным. В результате принимается решение о пересмотре отдельных положений Конвенции или продлении их действия.
В ходе консультаций стороны привлекают государства, не являющиеся членами Совета Европы, а также взаимодействуют с негосударственными организациями, представляющими интересы ряда специалистов: исследователей, ветеринарных врачей, заводчиков лабораторных животных, ассоциаций по защите прав животных, специалистов в области наук о животных, представителей фарминдустрии и других, которые присутствуют на собраниях рабочей группы в качестве наблюдателей.
В 1998 г. стороны, подписавшие Конвенцию, приняли решение о пересмотре Приложения А. Рабочая группа завершила пересмотр приложения А на 8-м собрании (22-24 сентября 2004 г.) и предоставила его на утверждение Многосторонней консультации сторон. 15 июня 2006 г. 4-я Многосторонняя консультация сторон по Европейской Конвенции об охране позвоночных животных, используемых в экспериментах и в других научных целях приняла пересмотренное приложение А к Конвенции. Настоящее приложение устанавливает требования к содержанию и уходу за животными, основанные на современных знаниях и надлежащей практике. Оно поясняет и дополняет основные положения статьи N 5 Конвенции. Цель настоящего приложения - помощь государственным органам, институтам и физическим лицам в их стремлении к достижению целей Совета Европы в данном отношении.
Глава "Общая часть" является руководством по размещению, содержанию и уходу за всеми животными, используемыми в экспериментальных и иных научных целях. Дополнительные рекомендации по наиболее часто используемым видам приведены в соответствующих разделах. В случае отсутствия информации в таком разделе следует соблюдать требования, приведенные в общей части.
Видоспецифичные разделы составлены на основании рекомендаций экспертных групп по работе с грызунами, кроликами, собаками, кошками, хорьками, нечеловекообразными приматами, сельскохозяйственными животными, мини-свиньями, птицами, амфибиями, рептилиями и рыбами. Экспертные группы предоставили дополнительную научно-практическую информацию, на основании которой были даны рекомендации.
Приложение А включает советы по дизайну помещений для содержания животных (вивариев), а также рекомендации и руководства по соблюдению требований Конвенции. Однако рекомендуемые стандарты помещений являются минимально допустимыми. В ряде случаев может потребоваться их увеличение, так как индивидуальные потребности в микроокружении могут существенно отличаться в зависимости от вида животных, их возраста, физического состояния, плотности содержания, целей содержания животных, например, для разведения или экспериментов, а также от длительности их содержания.
Пересмотренное приложение А вступило в силу через 12 месяцев после его принятия - 15 июня 2007 г.
Настоящий стандарт разработан с учетом нормативных положений Европейской конвенции о защите позвоночных животных, используемых в экспериментах и в других научных целях (ETS N 123), в частности приложения А и статьи N 5 Конвенции.
Серия ГОСТ "Руководство по содержанию и уходу за лабораторными животными" разработана на основе и включает все положения приложения А к Конвенции об охране позвоночных животных, используемых в экспериментах и в других научных целях, и, таким образом, эти стандарты гармонизированы с европейскими требованиями в данной области.
1 Область применения
Настоящий стандарт устанавливает общие требования к размещению, содержанию и уходу за лабораторными грызунами и кроликами, используемыми в учебных, экспериментальных и иных научных целях.
2 Нормативные ссылки
В настоящем стандарте использована нормативная ссылка на следующий стандарт:
ГОСТ 33215-2014 Руководство по содержанию и уходу за лабораторными животными. Правила оборудования помещений и организации процедур
Примечание - При пользовании настоящим стандартом целесообразно проверить действие ссылочных стандартов в информационной системе общего пользования - на официальном сайте Федерального агентства по техническому регулированию и метрологии в сети Интернет или по ежегодному информационному указателю "Национальные стандарты", который опубликован по состоянию на 1 января текущего года, и по выпускам ежемесячного информационного указателя "Национальные стандарты" за текущий год. Если ссылочный стандарт заменен (изменен), то при пользовании настоящим стандартом следует руководствоваться заменяющим (измененным) стандартом. Если ссылочный стандарт отменен без замены, то положение, в котором дана ссылка на него, применяется в части, не затрагивающей эту ссылку.
3 Термины и определения
В настоящем стандарте применены термины с соответствующими определениями - по ГОСТ 33215-2014 .
4 Видоспецифичные требования к содержанию грызунов
4.1 Введение
4.1.1 Мыши
Лабораторная мышь была выведена из дикой домовой мыши (Mus musculus), норного и лазающего зверька, ведущего преимущественно ночной образ жизни и строящего гнезда для регуляции условий микросреды, укрытия и репродукции. Мыши очень хорошо лазают, однако неохотно пересекают открытые пространства и предпочитают держаться ближе к укрытиям - стенам или другим объектам. Тип социальной организации сообществ мышей варьирует и определяется в основном плотностью популяции. У репродуктивно активных самцов наблюдается выраженное территориальное поведение, беременные и кормящие самки могут проявить агрессию при защите гнезд. Так как мыши, особенно альбиносы, имеют плохое зрение, они в основном полагаются на обоняние и оставляют мочевые метки на участке обитания. У мышей также очень острый слух, они чувствительны к ультразвуку. Существуют значительные различия в поведении мышей разных линий.
4.1.2 Крысы
Лабораторная крыса была выведена из серой крысы (Rattus norvegicus). Крысы - социальные животные, они избегают открытые пространства и используют мочевые метки для маркировки территории. Обоняние и слух у них развиты сильно, при этом крысы особо чувствительны к ультразвуку; дневное зрение - слабое, но у некоторых пигментированных линий при неярком свете зрение достаточно острое. Крысы-альбиносы избегают освещенности свыше 25 люкс (лк). Активность крыс повышается в ночные часы. Молодые животные очень любопытны и часто устраивают социальные игры.
4.1.3 Песчанки
Монгольская или Полуденная песчанка (Meriones sp.) - социальное животное, ведущее преимущественно ночной образ жизни, однако в лабораторных условиях сохраняющее активность и при дневном свете. В дикой природе песчанки роют норы с туннельными входами для защиты от хищников и поэтому в лабораторных условиях зачастую демонстрируют стереотипное рытье, если им не предоставлены условия для рытья нор.
4.1.4 Хомячки
Дикий предок лабораторного хомячка - Mesocricetus sp. - животное, ведущее преимущественно одиночный образ жизни. Самки хомячков крупнее и агрессивнее самцов и могут сильно травмировать своего партнера. Хомячки часто устраивают в клетке обособленное место для туалета и маркируют территорию секретами желез, находящимися по бокам тела. Самки хомячков часто поедают детенышей, чтобы уменьшить количество потомства.
4.1.5 Морские свинки
Дикие морские свинки (Cavia porcellus) - социальные, активно перемещающиеся грызуны, которые никогда не роют норы, однако селятся в укрытиях или используют чужие норы. Взрослые самцы могут быть агрессивны по отношению друг к другу, но в целом агрессия наблюдается редко. Морские свинки имеют обыкновение замирать, если услышат неожиданный звук. Они могут целой группой панически броситься прочь в ответ на резкое и неожиданное движение. Морские свинки особенно чувствительны к перемещениям с места на место и после этого могут замирать на тридцать и более минут.
4.2 Контроль среды обитания
4.2.1 Вентиляция - по ГОСТ 33215-2014 , п.4.1.
4.2.2 Температура
Грызунов следует содержать при температуре от 20°С до 24°С. При групповом содержании температура в клетках со сплошным дном чаще бывает выше комнатной, и даже при хорошо работающей вентиляции может превышать ее на 6°С. Материал для строительства гнезд и домики позволяют животным самостоятельно контролировать микроклимат. Особое внимание следует уделять поддержанию температуры в барьерных системах и там, где содержатся животные, лишенные шерстного покрова.
4.2.3 Влажность
Относительная влажность в помещениях для содержания грызунов должна поддерживаться в диапазоне от 45% до 65%. Исключением являются песчанки, которых следует содержать при 35-55% относительной влажности.
4.2.4 Освещение
Освещенность клетки должна быть низкой. Стеллажи для клеток должны иметь затемненную верхнюю полку для снижения риска дегенерации сетчатки глаза у животных, особенно альбиносов, содержащихся в клетках верхнего яруса. Для наблюдения за животными в темноте в период их активной фазы, можно использовать невидимый грызунами красный свет.
4.2.5 Шум
Так как грызуны очень чувствительны к ультразвуку и используют его для общения, необходимо свести к минимуму посторонние звуковые сигналы в данном диапазоне. Ультразвук (свыше 20 кГц), издаваемый лабораторным оборудованием, в том числе капающими кранами, колесиками тележек и компьютерными мониторами, может стать причиной аномального поведения и нарушений репродуктивного цикла у животных. Рекомендуется периодически измерять уровень шума в помещениях для содержания животных в широком диапазоне частот и в течение длительного времени.
4.2.6 Требования к системам тревожной сигнализации - по ГОСТ 33215-2014 , п.4.6.
4.3 Условия и факторы, влияющие на здоровье животных, приведены в ГОСТ 33215-2014 , п.6.1 и 6.4.
4.4.1 Размещение
Социальные животные должны содержаться постоянными и гармоничными группами, хотя в отдельных случаях, например, при совместном содержании взрослых самцов мышей, хомячков или песчанок, групповое содержание проблематично из-за внутривидовой агрессии.
Если существует риск возникновения агрессии или травм, животных можно содержать индивидуально. Следует избегать нарушения стабильных и гармоничных групп, так как это может вызвать очень сильный стресс у животных.
4.4.2 Обогащение среды обитания
Клетки и материалы, используемые для обогащения среды, должны позволять животным проявлять нормальное поведение и снижать вероятность возникновения конфликтных ситуаций.
Подстил и материалы для создания гнезд, а также укрытия - важные компоненты среды обитания грызунов, используемых для разведения, поддержания колонии или в эксперименте. Они должны присутствовать в клетке постоянно, за исключением случаев, когда это противоречит ветеринарным соображениям или нарушает благосостояние животных. В случае необходимости удаления таких материалов из клеток следует согласовывать это с персоналом по уходу за животными и компетентным лицом, наделенным консультативными полномочиями по вопросам благополучия животных.
Материал для строительства гнезд должен позволять животным создавать законченное закрытое гнездо. При отсутствии такой возможности следует предоставлять животным домики для гнездовья. Подстилочный материал должен впитывать мочу и использоваться животными для оставления мочевых меток. Материалы для создания гнезд необходимы мышам, крысам, хомякам и песчанкам, так как позволяют им создавать подходящее микроокружение для отдыха и размножения. Гнездовые домики и другие укрытия важны для морских свинок, хомяков и крыс.
Морским свинкам всегда следует предоставлять материалы, такие как сено, чтобы они могли жевать его и прятаться в нем.
Деревянные палочки для грызения и жевания могут использоваться в качестве обогащения среды обитания всех лабораторных грызунов.
Представители большинства видов грызунов пытаются разделить клетку на несколько зон - для потребления и хранения корма, отдыха и мочеиспускания. В основе такого разделения может лежать запаховая метка, а не физический барьер, но, тем не менее, частичные заграждения могут быть полезны, так как они позволяют животным инициировать контакты с соседями по клетке или, наоборот, избегать их. Для усложнения среды очень рекомендуется использовать дополнительные объекты. Тубы, коробки и стеллажи для лазания - примеры конструкций, успешно используемых для грызунов. Помимо этого, они позволяют увеличить полезную площадь клетки.
Песчанки нуждаются в большем пространстве, чем грызуны других видов. Площадь клетки должна позволять им заниматься строительством и/или использовать норы подходящего размера. Песчанкам необходим толстый слой подстила для копания, построения гнезд и рытья нор, длина которых должна достигать 20 см.
Следует предусмотреть использование полупрозрачных или слегка окрашенных клеток, обеспечивающих хороший обзор для наблюдения за животными без причинения им беспокойства.
Те же принципы в отношении качества и количества пространства, материалов для обогащения среды и других требований, изложенных в настоящем документе, должны применяться к барьерным системам, например, к системам индивидуально вентилируемых клеток (ИВК), хотя особенности их конструкции могут потребовать изменений в реализации вышеизложенных принципов.
4.4.3 Ограждения: размеры и структура пола
Клетки должны быть сделаны из материалов, легко поддающихся чистке, а их дизайн - обеспечивать проведение наблюдений без причинения беспокойства животным.
Как только молодые животные становятся активными, им требуется пропорционально больше пространства, чем взрослым особям.
4.4.3.1 Размеры
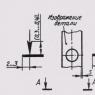
В этой и последующих таблицах, представляющих рекомендации по содержанию грызунов, "высота клетки" означает расстояние между полом и верхом клетки, при этом более 50% минимальной площади клетки должно иметь данную высоту до помещения туда материалов для создания богатых стимулами условий (обогащение среды).
При планировании процедур необходимо учитывать возможность роста животных, для того чтобы обеспечить их достаточным жизненным пространством (как подробно показано в таблицах 1-5) на весь период исследования.
4.4.3.2 Структура пола
Сплошной пол с подстилочным материалом или пол с перфорацией, предпочтительнее решетчатых или сетчатых полов. В случае использования клеток с решетчатыми или сетчатыми полами животных необходимо, если это не противоречит условиям эксперимента, обеспечить сплошными или покрытыми подстилом участками пола для отдыха. Для морских свинок альтернативой могут быть перекладины. Допускается не использовать подстилочный материал при проведении спаривания животных.
Сетчатые полы могут стать причиной получения серьезных травм, поэтому следует тщательно проверять их на наличие плохо закрепленных деталей и острых выступов и своевременно их устранять.
Самки на поздних сроках беременности, во время родов и кормления детенышей должны содержаться исключительно в клетках со сплошным дном и подстилочным материалом.
Таблица 1 - Мыши: минимальные размеры клеток (ограждений)
Мин. размер, см | Площадь/животное, см | Мин. высота, см |
||
В колонии и во время опытов | ||||
Разведение | ||||
Для моногамных пар (аутбредные или инбредные животные) или триад (инбредные). Для каждой доп. самки с пометом должно быть добавлено 180 см | ||||
В колонии у заводчика* Площадь пола клетки 950 см | ||||
Площадь пола клетки 1500 см | ||||
* В течение короткого периода после отлучения от матери мыши могут содержаться в группах большей плотности при условии их размещения в больших клетках с достаточно обогащенной средой, если при этом не наблюдается признаков нарушения их благосостояния, например: усиления агрессии, повышения заболеваемости и смертности, а также возникновения стереотипии и других нарушений нормального поведения, потери веса или прочих физиологических или поведенческих реакций, вызванных стрессом. |
||||
Таблица 2 - Крысы: минимальные размеры клеток (ограждений)
Мин. размер, см | Площадь/животное, см | Мин. высота, см |
||
В колонии и во время опытов* | ||||
Разведение | ||||
Самка с пометом; для каждого доп. взрослой крысы должно быть добавлено 400 см | ||||
В колонии у заводчика** Клетка - 1500 см | ||||
В колонии у заводчика** Клетка - 2500 см | ||||
* В продолжительных исследованиях животных следует обеспечивать клетками соответствующего размера, позволяющими содержать их социальными группами. Поскольку в таких исследованиях сложно предугадать плотность колонии к концу эксперимента, допустимы случаи содержания животных в условиях с меньшей площадью на одно животное, чем указано выше. В таком случае приоритет следует отдавать постоянству группы. ** В течение короткого периода после отлучения от матери крысята могут содержаться в группах большей плотности при условии их размещения в больших клетках с достаточно обогащенной средой, если при этом не наблюдается признаков нарушения их благосостояния, таких как усиление агрессии, повышение уровня заболеваемости и смертности, а также возникновение стереотипии, и других нарушений нормального поведения, потери веса или прочих физиологических или поведенческих реакций, вызванных стрессом. |
||||
Таблица 3 - Песчанки: минимальные размеры клеток (ограждений)
Мин. размер, см | Площадь/животное, см | Мин. высота, см |
||
В колонии (в стоке) и во время опытов | ||||
Разведение | ||||
Для моногамных пар или триад с пометом |
Таблица 4 - Хомячки: минимальные размеры клеток (ограждений)
Мин. размер, см | Площадь/животное, см | Мин. высота, см |
||
В колонии и во время опытов | ||||
Разведение | ||||
Самки или моногамные пары с пометом | ||||
В колонии у заводчика* | ||||
* В течение короткого периода после отлучения от матери хомячки могут содержаться в группах большей плотности при условии их размещения в больших клетках с достаточно обогащенной средой, если при этом не наблюдается признаков нарушения их благосостояния, например: усиления агрессии, повышения заболеваемости и смертности, а также возникновения стереотипии и других нарушений нормального поведения, потери веса или прочих физиологических или поведенческих реакций, вызванных стрессом. |
||||
Таблица 5 - Морские свинки: минимальные размеры клеток (ограждений)
Мин. размер, см | Площадь/животное, см | Мин. высота, см |
||
В колонии и во время опытов | ||||
Разведение | ||||
Пары с пометом; для каждой доп. самки должно быть добавлено 1000 см |
4.4.4 Кормление - по ГОСТ 33215-2014 , п.6.6.
4.4.5 Поение - по ГОСТ 33215-2014 , п.6.7.
4.4.6 Подстилочный, гнездовой и абсорбирующий материал - по ГОСТ 33215-2014 , п.6.8.
4.4.7 Чистка клеток
Несмотря на необходимость поддержания высоких гигиенических норм, может оказаться целесообразным оставлять животным некоторое количество запаховых меток. Следует избегать слишком частой чистки клеток, особенно при содержании беременных самок и самок с потомством, так как причиняемое беспокойство может стать причиной поедания потомства самкой или нарушения ее материнского поведения.
Решение о частоте проведения чистки клеток должно приниматься с учетом типа используемой клетки, вида животных, плотности колонии, способности вентиляционных систем поддерживать необходимое качество воздуха в помещении.
4.4.8 Обращение с животными
Следует стремиться к тому, чтобы причинять животным минимальное беспокойство и не нарушать условия их содержания, что особенно важно для хомячков.
4.4.9 Эвтаназия - по ГОСТ 33215-2014 , п.6.11.
4.4.10 Ведение учетных записей - по ГОСТ 33215-2014 , п.6.12.
4.4.11 Идентификация - по ГОСТ 33215-2014 , п.6.13.
5 Видоспецифичные требования к содержанию кроликов
5.1 Введение
В природных условиях кролики (Oryctolagus cuniculi) живут колониями. При содержании в неволе им необходимо предоставлять достаточно пространства с обогащенной средой, нехватка которого может привести к утрате нормальной двигательной активности и возникновению скелетных аномалий.
5.2 Контроль среды обитания
5.2.1 Вентиляция - по ГОСТ 33215-2014 , п.4.1.
5.2.2 Температура
Кроликов следует содержать при температуре от 15°С до 21°С. Температура в ограждениях со сплошным дном, где содержится группа кроликов, чаще всего бывает выше комнатной и даже при хорошо работающей системе вентиляции может превышать ее на 6°С.
Материал для строения гнезд и/или домики дают животным возможность самостоятельно контролировать микроклимат. Особое внимание следует уделять показаниям температуры в барьерных системах.
5.2.3 Влажность
Относительная влажность воздуха в помещениях для содержания кроликов не должна быть ниже 45%.
5.4.1 Размещение
Молодых кроликов и самок следует содержать гармоничными группами. Одиночное содержание допустимо, если его причинами являются благосостояние животного или ветеринарные соображения. Решение о возможности одиночного содержание животных в экспериментальных целях должно приниматься после консультации с персоналом по уходу за животными и ответственным лицом, наделенным консультативными полномочиями по вопросам физического и психического состояния животных. Взрослые некастрированные самцы могут проявлять территориальную агрессию, поэтому их не следует держать вместе с другими некастрированными самцами. Для группового содержания молодняка и взрослых самок кроликов прекрасно зарекомендовали себя напольные загоны с насыщенной средой обитания. Тем не менее, следует внимательно следить за группой, чтобы предупредить возможную агрессию. Идеально подходят для группового содержания однопометники, живущие совместно с момента отлучения их от матери. В тех случаях, когда невозможно групповое содержание, животные должны находиться как можно ближе друг к другу, в пределах видимости.
5.4.2 Обогащение среды обитания
Подходящими материалами для обогащения среды обитания кроликов являются грубые корма, блоки сена или палочки для жевания, а также конструкции, позволяющие укрыться.
В напольных загонах для группового содержания следует предусмотреть размещение разделительных барьеров и сооружений-укрытий, позволяющих животным наблюдать оттуда. При разведении кроликов следует обеспечивать гнездовым материалом и родильными ящиками.
5.4.3 Ограждения: размеры и структура пола
Преимущество следует отдавать прямоугольным клеткам, в которых должна быть приподнятая область, площадью не превышающая 40% общей площади пола. Полка должна позволять животным сидеть и лежать, а также свободно двигаться под ней. Хотя высота клетки должна позволять кролику сидеть, не касаясь кончиками поднятых ушей потолка, такое же требование к приподнятой площадке не предъявляется. Если есть достаточные научные или ветеринарные основания для того, чтобы не размещать в клетке такую полку, то площадь клетки должна быть на 33% больше для одного кролика и на 60% - для двух кроликов. Там, где это возможно, кроликов следует содержать в загонах.
5.4.3.1 Размеры
Таблица 6 - Кролики старше 10 недель: минимальные размеры ограждений
Мин. площадь для 1-2 социально подходящих друг другу животных, см | Мин. высота, см |
|
Данные таблицы 6 относятся и к клеткам, и к вольерам. В клетках должна присутствовать приподнятая площадка (см. таблицу 9). Вольеры должны быть оборудованы разделительными барьерами, позволяющими животным инициировать социальные контакты или избегать их. Для каждого с 3-го по 6-го подсаживаемого в вольер кролика к площади вольера следует добавить 3000 см, а для каждого последующего - 2500 см.
Таблица 7 - Самка кролика с детенышами: минимальные размеры ограждений
Вес самки, кг | Мин. размер, см | Дополнительное пространство для гнезд, см | Мин. высота, см |
Как минимум за 3-4 дня до родов самке следует предоставить отдельный отсек или родильный ящик, в котором она может построить гнездо. Лучше, если родильный ящик будет размещен вне места постоянного содержания самки. Следует также предоставить солому или другой материал для обустройства гнезда. Ограждение для разведения кроликов должно быть организовано таким образом, чтобы самка могла уйти от своих подросших крольчат, способных покинуть гнездо, в отдельный отсек, укрытие или на приподнятую площадку. После отлучения от матери кроликов из одного помета следует как можно дольше содержать вместе в том же ограждении, где они родились.
В ограждении для разведения допускается содержать до восьми однопометников до достижения ими возраста семи недель. Пять однопометников 8-10-недельного возраста можно содержать на минимально допустимой площади ограждения.
Таблица 8 - Кролики моложе 10-недельного возраста: минимальные размеры ограждений
Возраст, нед. | Мин. размер клетки, см | Мин. площадь/животное, см | Мин. высота, см |
Данные таблицы 8 относятся и к клеткам, и к вольерам. Вольеры должны быть оборудованы разделительными барьерами, позволяющими животным инициировать социальные контакты или избегать их. После отлучения от матери однопометников следует как можно дольше содержать вместе в том же ограждении, где они родились.
Таблица 9 - Кролики старше 10-недельного возраста: оптимальные размеры приподнятой площадки в ограждениях, имеющих размеры, указанные в таблице 6.
Возраст, нед. | Оптимальный размер площадки, смсм | Оптимальная высота площадки от пола клетки, см |
|
Для обеспечения правильного использования приподнятой площадки и ограждения в целом в таблице 9 приводятся оптимальные размеры и высота, на которой находится площадка. Допускается отклонение до 10% в сторону уменьшения или увеличения заданных размеров. Если имеются достаточные научные или ветеринарные основания для того, чтобы не размещать в ограждении такую полку, то площадь ограждения должна быть на 33% больше для одного кролика и на 60% - для двух кроликов с целью обеспечения их пространством для нормальной двигательной активности и возможностью избегать контакта с доминирующей особью.
Для кроликов не старше 10-недельного возраста оптимальные размеры приподнятой площадки составляют 55 см25 см, а высота ее над уровнем пола должна позволять животным пользоваться и площадкой, и пространством под ней.
5.4.3.2 Дно клеток
Не следует использовать ограждения с решетчатыми полами без обеспечения участка, достаточного для единовременного отдыха всех животных. Сплошные полы с подстилочным материалом или полы с перфорацией лучше решетчатых или сетчатых.
МКС 13.020.01
Ключевые слова: лабораторные животные, грызуны, кролики
Электронный текст документа
подготовлен АО "Кодекс" и сверен по:
официальное издание
М.: Стандартинформ, 2016
Под лабораторными животными понимаются любые позвоночные, которые применяются для научных исследований, обучения или испытаний. Условно их делят на традиционные, т. е. наиболее часто используемые в экспериментах, и нетрадиционные, которые нечасто используются в биомедицинских исследованиях. К традиционным относятся лабораторные мыши, крысы, кролики, морские свинки, хомяки, кошки, собаки, обезьяны и др. К нетрадиционным - песчанки, суслики, рыбы, опоссумы, броненосцы и др.
Зоогигиенические требования к устройству вивария. Помещение, где под контролем специалистов лабораторного животноводства осуществляется содержание, размножение животных, используемых для экспериментальных (научных) или учебных целей, а также для практики здравоохранения, называют виварием (от лат. \ivus - живой).
Выбор технологии содержания и разведения лабораторных животных, а также планирование и проектирование помещений для животных определяется микробиологической категорией (статусом) животных.
Помещения, предназначенные для содержания животных, должны обеспечивать им нормальную жизнедеятельность. Любые отклонения от нормы в среде, окружающей животное, немедленно сказываются на его внутреннем состоянии. Ого неизбежно приводит к искажению результатов научных исследований.
Таким образом, требования, предъявляемые к помещениям для животных, теснейшим образом связаны с получением объективных (достоверных) результатов экспериментов и их воспроизводимости в будущем.
Правильно спроектироваяный, хорошо сконструированный, построенный и содержащийся в должном состоянии виварий составляет важный элемент правильного содержания и использования животных и облегчает эффективную, экономичную и безопасную эксплуатацию. Конструкция и размер вивария определяются масштабом исследовательской работы с животными в данном научном учреждении, видом содержащихся в нем животных, расположением вивария по отношению к другим здания» и географической зоной, где оно находится.
Необходимым требованием обеспечения правильного содержания животных и охраны здоровья обслуживающего персонала является отделение помещений, где содержатся животные, от служебных помещений.
Продуманное планирование позволяет разместить виварий рядом или вблизи с научно-исследовательской лаборатори-
1 - помещение для приема животных; 2 - гсмеще- ние для приемного контроля животных; 3 - поие- щение для наблюдения животных; 4 - административное и вспомогательное помещение: 5 - раздевалка; 6 - санузел; 7 - чистый коридор; 8 - склад 9 - «предпроцедурное» помещение; 10 - помещение для содержания животных: 11 - запасное подготовительное помещение; 12 - помещение для койки; 13 - машинное помещение; 14- помещение для сжигания отходов; 15 - грязный коридор; 1Б- помещение для стерилизадии.
ей, разделив их барьерами типа тамбура, коридора или этажа. Виварий должен состоять из: 1) помещения для приема животных; 2) карантинного отделения;
- комнат для содержания животных;
- манипуляционной; 5) операционной; 6) ветеринарно-диагностического кабинета и других вспомогательных служб.
В виварии обеспечивают изоляцию поступивших и находящихся в карантине и в изоляторе животных, изоляцию чистых» и «грязных» потоков, естественное и искусственное освещение, отопление, непрерывную вентиляцию, снабжение холодной и горячей водой, канализацией.
При выборе строительных материалов предпочтение следует отдавать наиболее эффективным и облегчающим уборку помещений. Для отделки внутренних поверхностей необходимо использовать прочные, водоотталкивающие, огнестойкие и бесшовные материалы. Поверхности должны быть высокоустойчивы к действию чистящих механических и химических средств, обработке струей воды под давлением и к ударам. При покрытии поверхностей, с которыми могут соприкасаться животные, краской и плиткой, нужно предусмотреть использование нетоксических материалов. При строительстве сооружений на открытом воздухе следует применять материалы, устойчивые к атмосферным воздействиям и легко поддающиеся уборке.
Коридоры должны быть достаточно широкими для беспрепятственного прохода персонала и доставки оборудования. Для большинства сооружений рекомендуются коридоры шириной 1,8-2,4 м.
По соображениям безопасности двери должны открываться внутрь помещения, где содержатся животные; однако, если возникнет необходимость открывания дверей в коридор, нужно предусмотреть сооружение тамбура. С точки зрения безопасности и других причин предпочтение следует отдавать дверям со смотровыми окнами. Двери должны быть достаточно большими (приблизительно 105 х 210 см), чтобы обеспечить свободный доступ для кормушек и оборудования.
Если необходимо или желательно ограничить доступ в какие-то помещения (например, при использовании опасных веществ), двери следует оборудовать замками. При этом конструкция дверей должна предусматривать возможность их открывания изнутри без ключа.
Полы должны быть водоотталкивающими, неабсорбирующими, устойчивыми к ударным воздействиям и сравнительно гладкими.
Стены должны быть гладкими, водоотталкивающими, неабсорбирующими и резистентными к ударам. В них не должно быть трещин, незаделанных отверстий, через которые проходят коммуникации, или плохо заделанных стыков с дверьми, потолками, полами и углами. Материалы, которыми покрыты поверхности стен, должны быть достаточно стойкими и выдерживать обработку детергентами и дезинфицирующими препаратами, а также водой под мощным давлением.
Потолки должны быть гладкими, водонепроницаемыми и не иметь дефектных стыков. Материалы, которыми покрыты потолки, должны выдерживать обработку моющими и дезинфицирующими препаратами. Потолки, покрытые штукатуркой или огнестойкой сухой штукатуркой, должны быть обработаны уплотняющим материалом и окрашены моющейся краской. Потолки, образуемые бетонным полом верхнего этажа, считаются приемлемыми, если они гладкие, обработаны уплотняющими прокладками и покрашены.
Помещения для обработки или хранения кормов или их ингредиентов должны содержаться в чистоте и быть защищены от проникновения вредителей. Корма следует хранить не на полу, а на поддонах, полках или тележках.
Конструкция и размещение кормушек должны обеспечивать удобный доступ к корму и сводить до минимума возможность его загрязнения мочой и фекалиями. В обычных условиях животные должны иметь свободный доступ к чистой питьевой воде в соответствии с их индивидуальными потребностями.
Подстилка для животного является контролируемым фактором окружающей среды, который может влиять как на экспериментальные данные, так и на состояние животного. Чтобы обеспечить сохранность качества и свести до минимума возможность контаминации подстилочных материалов, их следует транспортировать и хранить не на полу, а на поддонах, полках или тележках. Частота и интенсивность проведения уборки и дезинфекции зависят от требований, предъявляемых к здоровой среде обитания животного с учетом его нормального поведения и физиологических характеристик.
Частота санитарной обработки клеток, стеллажей и вспомогательного оборудования определяется типом используемых клеток и принятыми методами ухода за животными, включающими регулярную ручную или автоматическую смену подстилки и регулярное промывание струей воды поддонов. Клетки и сопутствующее оборудование должны подвергаться санитарной обработке не реже одного раза в две недели. Клетки со сплошным полом, бутыли с водой и трубки-поилки обычно требуют санитарной обработки, по крайней мере, раз в неделю.
Дезинфекция оказывается достаточно эффективной при мойке и ополаскивании водой, нагретой до 60-80°С или выше.
Инвентарь, используемый при уборке, должен быть закреплен за определенными
помещениями, и его не следует переносить из одного помещения в другое. Сам инвентарь следует регулярно чистить; причем он должен быть изготовлен из коррозионно-устойчивых материалов.
Профилактика заболеваний является важнейшим элементом ветеринарного обеспечения животных. Эффективные программы профилактических мероприятий способствуют повышению научной ценности животных, поскольку они позволяют сохранить их здоровье и свести до минимума вероятность изменения их состояния, обусловленную заболеваниями. Программы профилактических мероприятий включают различные комбинации правил, процедур и методов, связанных с карантином и стабилизацией здоровья животных, а также с раздельным содержанием животных в зависимости от вида, источника поступления и состояния здоровья.
Карантин предполагает содержание вновь поступивших животных отдельно от животных, уже находящихся в виварии, до полного определения состояния здоровья и, возможно, микрофлоры вновь поступивших животных.
К раздельному содержанию животных одного и того же вида можно прибегать в тех случаях, когда животные, поступившие из разных центров или источников, являются носителями различных патогенных микроорганизмов (Сидорчук А. А., Глушков А. А., 2002).
После карантина (мыши, крысы - 10 суток, собаки - 30 суток, остальные животные - 21 сутки) животных маркируют (мышей и крыс - окраской, кроликов - надеванием на ухо бирки с номером, птиц - кольцеванием), осматривают, взвешивают, замеряют температуру, частоту дыхания, пульс. Если отклонения от нормы отсутствуют, животное берут в опыт и переводят в специальное помещение. Вышедших из опыта животных подвергают безболезненному умерщвлению (эвтаназии). Мелких животных умерщвляют декапитацией или ингаляцией хлороформа (эфира), кроликов - воздушной эмболией, крупных животных - электрическим током.
Оборудование вивария и микроклимат. Кондиционирование воздуха является эффективным средством регулирования температуры и влажности воздуха. Конструкция систем обогрева, вентиляции и кондиционирования воздуха должна обеспечивать их надежность, удобство эксплуатации и экономию электроэнергии.
Относительная влажность обычно поддерживается в пределах 30-70% в течение всего года. На случай частичного отказа системы обогрева, вентиляции и кондиционирования воздуха необходимо предусмотреть аварийную систему, которая обеспечила бы поддержание уровней температуры и влажности в приемлемом диапазоне.
В некоторых случаях рекомендуется использование фильтров для очистки воздуха, поступающего в помещения для содержания животных, проведения экспериментальных процедур и хирургических манипуляций.
Электрическая система должна быть безопасной и обеспечивать адекватное освещение, иметь достаточное количество розеток и гарантировать достаточную силу тока для специального оборудования. На случай отключения электричества необходимо предусмотреть альтернативный или аварийный источник электроэнергии для обеспечения функционирования критически важных систем или вспомогательных систем (например, морозильников, вентилируемых стеллажей и изоляторов) в помещениях для животных, операционных блоках и других важных зонах.
Зоны для хранения отходов должны быть отделены от других хранилищ. Для хранения трупов животных и их тканей обязательно иметь холодное помещение
С холодильнии камерии, отделенное нт других холодных комнат; в таком помещении температура не должна превышать 7°С, чтобы исключить возможность разложения отходов и трупов животных.
При эксплуатации вивария большое значение имеет регулирование уровня шума. В отношении защиты от шума кирпичные стены представляются более эффективными, чем металлические или гипсовые, поскольку благодаря своей плотности они обладают меньшей звукопроницаемостью. В некоторых ситуациях с целью уменьшения уровня шума можно использовать поддающиеся обработке звукоизолирующие материалы, прикрепляемые к стенам или потолкам. Определенное внимание следует уделить снижению уровня шума, генерируемого работающей аппаратурой, особенно в ультразвуковом диапазоне.
В виварии необходимо предусмотреть специальную единую зону для санитарной обработки клеток и вспомогательного оборудования. Обычно для мойки клеток рекомендуется использовать механические моечЕые машины, которые следует выбирать с учетом типа клеток и другого оборудования.
Первичное ограждение (обычно клетка, загон или стойло) ограничивает непосредственную среду обитания животного. Приемлемые первичные ограждения:
- удовлетворяют нормальным физиологическим и поведенческим потребностям животного, включая мочеиспускание и дефекацию, поддержание температуры тела, нормального характера движений и поз, а также, по показаниям, размножение;
- обеспечивают социальные взаимоотношения и установку иерархических отношений внутри или между ограждениями;
- дают возможность животным оставаться чистыми и сухими (в соответствии с потребностями данного вида);
- ооеспечивают одслошпую вентиляцию; обеспечивают животным доступ к пище и воде, а также позволяют легко заполнять, менять, обслуживать и чистить посуду, где содержится корм и вода;
- обеспечивают безопасность животного, т. е. исключают возможность его бегства, случайного попадания (целиком или конечностями) в щели или застревания между противоположными поверхностями;
- не имеют острых краев или выступов, которые могут травмировать животное;
- дают возможность наблюдать за животными, практически не вызывая их беспокойства.
Все первичные ограждения должны поддерживаться в хорошем состоянии, чтобы предотвращать бегство или травмирование животных, способствовать их физическому комфорту и облегчать их
санитарную обработку и обслуживание. Ржавеющее или окисленное оборудование, которое угрожает здоровью или безопасности животных, должно ремонтироваться или заменяться новым.
Некоторые системы содержания животных имеют специальные клетки и вентиляционное оборудование, в том числе клетки с встроенными фильтрами, вентилируемые клетки, изоляторы и небольшие боксы. В целом назначение таких систем состоит в сведении до минимума распространения возбудителей инфекционных заболеваний воздушным путем между клетками или группами клеток.
Грызунов часто размещают на полу из проволочной сетки, которая облегчает соблюдение санитарных норм, позволяя собирать мочу и фекалии в расположенные под ней поддоны. Однако по некоторым данным, для грызунов предпочтительнее оказываются клетки с твердым дном и подстилом. Для содержания других видов животных, например собак и приматов, часто используются полы с виниловым покрытием.
 Температура и относительная влажность окружающей среды могут зависеть от конструкции помещения и условий размещения животных. К факторам, которые могут способствовать колебаниям температуры и влажности, относятся конструкция и материалы, из которых изготовлены ограждения, использование фильтра с надставкой, количество животных в клетке, приточная вентиляция ограждения, частота смены подстилочного материала и его состав.
Температура и относительная влажность окружающей среды могут зависеть от конструкции помещения и условий размещения животных. К факторам, которые могут способствовать колебаниям температуры и влажности, относятся конструкция и материалы, из которых изготовлены ограждения, использование фильтра с надставкой, количество животных в клетке, приточная вентиляция ограждения, частота смены подстилочного материала и его состав. В некоторых ситуациях, например при послеоперационном восстановлении животного, содержании цыплят в течение первых дней после вывода, содержании некоторых грызунов, лишенных волосяного покрова, и новорожденных особей отдельно от матери, может потребоваться поддержание более высокой температуры. Диапазон повышения температуры зависит от условий содержания (Берг- хоф П. К., 1998).
При содержании животных в замкнутом пространстве диапазон суточных колебаний температуры должен быть сведен до минимума с тем, чтобы избежать многократных воздействий на метаболизм и поведение животных, изменяющихся для компенсации сдвигов температуры окружающей среды. Уровень относительной влажности также должен контролироваться, но в более широком диапазоне, чем температура (приемлемый диапазон
Шум, источником которого являются животные и обслуживающий их персонал, служит непременной характеристикой действующего вивария. Поэтому при проектировании и эксплуатации вивария необходимо учитывать возможность регулирования уровня шума.
Животных, создающих много шума, например собак, свиней, коз и приматов, следует помещать на расстоянии от тихих животных, например грызунов, кроликов и кошек. Воздействие шума с уровнем интенсивности, превышающим 85 дБ, может оказать влияние как на слуховой аппарат, так и на другие органы. Многие виды животных обладают способностью слышать звуки такой частоты, которые не доступны человеку, поэтому нужно обращать особое внимание на потенциальное воздействие аппаратуры, например видеоаппаратуры, и материалов, продуцирующих шум в диапазоне слышимости находящихся поблизости животных. В виварии нельзя пользоваться радиоаппаратурой, будильниками и другими приборами, создающими шум, если только они не входят в состав утвержденной экспериментальной аппаратуры или оборудования, предназначенного для обогащения среды обитания животных.
В зависимости от вида животных и направления их использования структура среды обитания должна включать планки для отдыха, полки или насесты, игрушки, кормушки и поилки, материал для строительства гнезд и нор, туннели, качели и другие предметы, которые предоставляют животным большие возможности для проявления видоспецифичного поведения, принятия нормальных поз и способствуют их благополучию.
Размещение и транспортировка животных. При размещении животных необходимо стремиться к тому, чтобы создать максимально благоприятные условия для видоспецифичного поведения и свести до минимума стрессовое воздействие. Для социальных видов животных такое требование обычно предполагает их размещение совместимыми парами или группами. Персонал, осуществляющий уход за животными, должен выработать стратегию наиболее целесообразного размещения животных, обеспечивающего их здоровье и благополучие, а также соответствующего задачам эксперимента.
Мышей, морских свинок, кроликов, крыс, хомяков, кур размещают в находящихся на стеллажах клетках, строго соблюдая плотность посадки, собак и обезьян - в отдельных кабинах, кошек - в вольерах. Дно клеток покрывают тонким слоем опилок или стружек, предварительно простерилизованных при 150-180°С в течение 15-20 минут. В поилках клеток должна быть питьевая вода, отвечающая требованиям СанПиН. Необходимо соблюдать нормы и режим кормления. Посуду для воды и кормов следует регулярно дезинфицировать, мыть и ополаскивать.
Потребности животных в занимаемом пространстве определяются разными факторами; при этом учет только массы или площади поверхности тела животного является недостаточным.
Для некоторых видов животных более благоприятным является наличие перегородок (например, грызуны, для которых характерен тигмотаксис), укрытий или сложной структуры клеток (например, кошки и шимпанзе), а не простое увеличение площади (Рахманов А. И., 2002).
Такие показатели состояния животных, как здоровье, размножение, рост, поведение, активность и использование ими пространства могут служить оценкой соответствия их размещения. Как минимум, животное должно иметь достаточно места, чтобы поворачиваться и принимать нормальные позы, иметь свободный доступ к кормушкам и поилкам, а также достаточное и свободное (покрытое чистой подстилкой) пространство, где
оно может удобно расположиться и отдыхать. В клетке для кошек необходимо установить приподнятую над полом платформу для отдыха. Такие платформы или выступы часто желательно устраивать для собак и приматов. Пространство, занимаемое кормушками, поилками, устройствами для туалета или другими приспособлениями, которые не предназначены для передвижения или отдыха, не должно входить в площадь пола.
Высота ограждений может иметь большое значение для нормального поведения и приспособления некоторых видов животных. При расчете высоты клеток нужно принимать во внимание типичные позы животного и достаточное место для обязательных элементов клетки, например кормушек, поилок, ванн с водой. Приматы некоторых видов используют вертикальные пространства клетки в большей степени, чем ее пол. Для их хорошего самочувствия важно предоставлять им возможность высоко взбираться на ветку и использовать вертикальное пространство, достаточное для размещения всего тела над полом клетки.
При расчете производственных площадей необходимо исходить из следующих нормативов размещения животных в клетках (табл. 55).
В табл. 56 приводятся рекомендуемые размеры клеток для других обычно используемых в лабораторных экспериментах животных. Эти данные основаны на потребностях животных при индивидуальном содержании. Размеры клеток могут быть пересмотрены при необходимости обогащения среды обитания или содержания животных с массой, превышающей указанную в таблице. При групповом содержании животных площадь общего пространства не является обязательно суммой величин, рекомендуемых для индивидуального содержания животных. При групповом содержании животных расчеты должны основываться на потребностях и поведенческих характеристиках животных данного вида, совместимости особей, количестве животных, а также задачах, которые ставятся при их размещении.
Высших обезьян массой более 50 кг лучше содержать в помещениях из кирпича, бетона и в проволочных ограждениях, а не в обычных клетках.
Все животные должны приобретаться законным путем. Если собаки и кошки поступают от дилеров или станций отлова животных, то таких животных следует осмотреть на предмет их возможной идентификации. Подобная проверка может выявить факт, что данное животное было домашним; в таком случае следует установить его владельца.
Использование специально выведенных экспериментальных животных возможно, если оно диктуется задачами исследования, обучения или испытаний.
Любые перемещения животных, в том числе внутри вивария, следует должным образом координировать с тем, чтобы свести до минимума время перевозки
| Вид животных | №1асса, кг | Площадь пола на одно животное, м1 | Высота от пола до потолка клетки, см |
| Кролики | ДоЗ | 0,1 | 35,6 |
| ДО 4 | 0,3 | 35,6 |
|
| до 5 | 0,4 | 35,6 |
|
| более 5 | 0,5 | 35,6 |
|
| Кошки | до 4 | 0,3 | 61,0 |
| более 5 | 0,4 | 61,0 |
|
| Собаки | до 15 | 0,7 | - |
| до 30 | 1,1 | - |
|
| более 30 | 2,2 | - |
|
| Обезьяны (включая павианов) |
|||
| 1 особь | до 1 | 0,1 | 50,8 |
| 2 особи | доЗ | 0,3 | 76,2 |
| 3 особи | д О о | 0,4 | 76,2 |
| 4 особи | до 15 | 0,5 | 81,3 |
| 5 особей | до 25 | 0,7 | 91,4 |
| 6 особей | до 30 | 0,9 | 116,8 |
| 7 особей | более 30 | 1,4 | 116,8 |
| Человекообразные обезьяны |
|||
| 1 особь | до 20 | 0,9 | 139,7 |
| 2 особи | до 35 | 1,4 | 152,4 |
| 3 особи | более 35 | 2,3 | 213,4 |
| Голуби | - | 0,1 | - |
| Перепела | - | 0,02 | - |
| Куры | д о 0,25 | 0,02 | - |
| до 0,5 | 0,05 | - |
|
| до 1,5 | 0,1 | - |
|
| до 3,0 | 0,2 | - |
|
| более 3,0 | 0,3 | - |
|
и риск передачи зоонозов, защитить животных от воздействия экстремальных условий окружающей среды, исключить слишком большую скученность животных, обеспечить при необходимости их доступ к корму и воде и предохранить от физических травм. Связанный с транспортировкой стресс является неизбежным, однако он может быть сведен до минимума при должном внимании к перечисленным выше факторам. Каждую партию животных необходимо проверять на соответствие требованиям получателя и на наличие клинических признаков заболеваний, при этом животных следует помещать в карантин и стабилизировать их состояние с помощью процедур, соответствующих данному виду и условиям.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАНИЯ
- Какие способы содержания собак и ухода за ними вы знаете?
- В чем заключаются особенности содержания кошек и ухода за ними?
- Какие гигиенические требования предъявляются при транспортировке собак и кошек?
- В чем заключается гигиена выращивания молодняка собак и кошек?
- Какие гигиенические требования к кормлению и поению собак и кошек?
- Какие требования предъявляют к выбору места для вивария и его устройству?
- В чем заключаются зоогигиенические требования к вивариям?
- Как обеспечивается оптимальный микроклимат в виварии?
- Какие санитарно-гигиенические требования предъявляют при содержании лабораторных животных?
РД-АПК 3.10.07.02-09
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА
РОССИЙСКОЙ ФЕДЕРАЦИИ
Москва 2009
Разработаны: канд. с.-х. наук, ст. науч. сотр. П.Н. Виноградовым, канд. техн. наук С.С. Шевченко, О.Л. Седовым, Е.С. Гарафутдиновой, М.Ф. Малыгиным (НПЦ «Гипронисельхоз»); д-р вет. наук, проф. В.Г. Тюриным (ГНУ ВНИИВСГЭ)
ВНЕСЕНЫ: НПЦ «Гипронисельхоз».
УТВЕРЖДЕНЫ И ВВЕДЕНЫ В ДЕЙСТВИЕ: заместителем Министра сельского хозяйства Российской Федерации А.И. Беляевым 1 декабря 2009 г.
РАЗРАБОТАНЫ ВПЕРВЫЕ.
Дата введения 15.12.2009
1 Общие положения
1.1. Настоящие методические рекомендации распространяются на все научно-исследовательские организации и учебные заведения АПК России независимо от их организационно-правовой формы, использующие в своей работе лабораторных (экспериментальных, подопытных) животных.
В соответствии с Федеральным законом «О техническом регулировании » (принят Государственной Думой 15 декабря 2002 г. и одобрен Советом Федерации 18 декабря 2002 г.) до принятия соответствующих регламентов техническое регулирование в области принятия ветеринарно-санитарных мер осуществляется в соответствии с Законом Российской Федерации «О ветеринарии» (утвержден 14 мая 1993 г., № 4979-1).
1.2. Методические рекомендации распространяются как на вновь проектируемые объекты для содержания и работы с лабораторными животными - экспериментально-биологические клиники, виварии и др., так и на действующие и реконструируемые.
1.3. Объекты для содержания и работы с лабораторными животными являются научно-вспомогательными подразделениями научно-исследовательских организаций, учебных заведений и создаются для содержания и при необходимости для разведения лабораторных животных, используемых в экспериментальных работах и исследованиях. На этих объектах может проводиться также и самостоятельная разработка отдельных научных вопросов.
1.4. Изложенные в данных методических рекомендациях нормативы и требования по проектированию, строительству и эксплуатации объектов для содержания лабораторных животных направлены на обеспечение безопасности работающего с животными персонала и населения в целом от возникновения антропозаонозов и других заболеваний.
1.5. Разработка, согласование, утверждение и состав проектной документации на строительство объектов для содержания лабораторных животных осуществляются в соответствии с требованиями СНиП 11.01-2003 .
1.6. Объект для содержания лабораторных животных (далее виварий) размещается в отдельно стоящем здании (комплексе зданий) или на верхних этажах лабораторных корпусов ветеринарных государственных научных учреждений, а также на территории учебных заведений.
1.7. Виварии должны быть обеспечены водой питьевого качества, в том числе горячей, электроэнергией, оборудованы канализацией (трубы диаметром не менее 100 мм), приточной и вытяжной вентиляцией, отоплением, охранной и пожарной сигнализацией, иметь удобные подъездные пути.
1.8. Расстояние между отдельно стоящим зданием вивария и сооружениями научно-исследовательских учреждений, в состав которых входит настоящий виварий, должно быть не менее расстояния противопожарных разрывов, установленных действующими правилами пожарной безопасности в Российской Федерации.
1.9. Отдельно стоящие здания вивариев должны быть огорожены глухим забором и отделены от жилого массива санитарно-защитной зоной. Территория должна быть озеленена.
Размеры санитарно-защитной зоны определяются требованиями СаНПиН 2.2.1/2.1.1.1200-03 .
1.10. Размеры санитарно-защитной зоны для вивариев, расположенных в отдельно стоящих административных, производственных зданиях и имеющих изолированный выход, согласовываются в каждом конкретном случае с органами государственного санитарного и ветеринарного надзора.
2. Состав, взаиморасположение и нормы площади помещений вивариев
2.1. В состав каждого вивария должны быть включены помещения, запроектированные в соответствии с действующими строительными нормами и правилами с соблюдением действующих ветеринарно-санитарных требований и зоогигиенических нормативов, в том числе:
комната обслуживающего персонала с индивидуальными шкафчиками для спецодежды;
помещения для приема и карантинирования вновь поступающих в виварий животных;
изолятор;
помещения для содержания подопытных животных (отдельные для каждого вида) или (по согласованию с органами государственного ветеринарного и санитарного надзора) разделенные на секции по видам животных;
стерилизационная или бокс для работы исследователей с незараженными животными, с помещением для вскрытия животных и холодильником для временного хранения трупов;
изолированные помещения для содержания подопытных животных, зараженных культурами возбудителей особо опасных инфекций или радиоактивными веществами (раздельно) с операционной при каждом изолированном помещении, имеющей холодильник и необходимое оборудование для заражения и вскрытия животных;
кормокухня для приготовления кормов (должна быть оборудована плитой и холодильником);
дезинфекционно-моечное отделение для мойки горячей водой, дезинфекции и сушки клеток и другого инвентаря;
склад чистого (обеззараженного) запасного инвентаря: клеток, поилок и др.;
санитарный блок (душевая и туалет);
помещение, оборудованное печью для сжигания трупов животных;
общая холодильная камера для хранения трупов животных;
склад кормов;
склад подстилки;
в отдельном помещении или в отдельно расположенном здании - технический узел для кондиционеров, вентиляционных, электротехнических и других специальных установок.
2.2. В каждом виварии должно быть помещение для приема поступающих животных. В вивариях, в которых содержат мелких грызунов, перед приемным отделением устанавливается утепленный тамбур, в который въезжает и разгружается машина с прибывшими животными.
При размещении вивария на верхних этажах лабораторных корпусов приемное отделение и утепленный тамбур располагаются на первом этаже лабораторного корпуса и связываются с виварием лифтом, используемым только для подъема лабораторных животных.
2.3. Помещение приема представляет собой комнату площадью 12,5 - 18 м 2 с естественным и искусственным освещением в соответствии с требованиями .
Высота всех помещений вивария составляет 3 - 3,5 м.
2.4. Помещение карантина состоит из нескольких изолированных комнат площадью 12,5 - 18 м 2 и изолируется от помещений, в которых содержатся животные, прошедшие карантин и поступающие для проведения экспериментов.
2.5. К помещениям карантина примыкает помещение изолятора для больных животных и животных с подозрением на заболевания. Площади комнат изолятора аналогичны площадям комнат для карантина.
2.6. Помещения, предназначенные для содержания подопытных животных, могут выходить в один общий коридор или располагаться между двумя коридорами и иметь выходы в каждый из них. При однокоридорной планировке «грязные» и «чистые» службы располагают в разных концах коридора.
При двухкоридорной системе по одному коридору («чистому») поступают корма, прошедшие карантин животные, входят перед началом работы с животными сотрудники в чистой спецодежде и сменной обуви. По другому («грязному») коридору удаляют несъеденные корма и навоз, выносят трупы животных, выходят сотрудники после работы с животными.
При невозможности изоляции «грязных» и «чистых» потоков допускается использование одного и того же помещения для той или другой цели при условии, что оно будет дезинфицироваться каждый раз после прохождения по нему «грязного» потока.
2.7. Площадь помещений для содержания отдельных видов подопытных животных составляет 12,5 - 18 м 2 ; площадь помещения для содержания подопытных животных, разделенная на секции, определяется расчетом.
2.8. Площадь стерилизационной или бокса для работы исследователей с незараженными животными определяется расчетом, исходя из специфики предполагаемой работы.
2.9. Площади изолированных помещений для работы с подопытными животными, зараженными возбудителями особо опасных инфекций, и для работы с подопытными животными, зараженными радиоактивными веществами, а также площади операционных при каждом изолированном помещении определяются расчетом, исходя из условий применяемого технологического и специального оборудования для проведения необходимых манипуляций.
2.10. Общая площадь помещений, занимаемая кормокухней, дезинфекционно-моечным отделением и складом чистого запасного инвентаря, должна составлять примерно 50 % от общей площади помещений, занятых животными (в крупных вивариях этот процент может быть несколько уменьшен).
Кормокухня состоит из двух смежных помещений, предназначенных для переработки и приготовления кормов. Каждое помещение должно иметь выход в коридор.
Дезинфекционно-моечное отделение (одно или несколько) состоит из двух комнат, соединенных проходным автоклавом или проходной сухожаровой камерой.
Устройство дезинфекционно-моечного отделения должно предусматривать различную последовательность его работы:
при наличии инфицированного материала - предварительную стерилизацию инвентаря и подстилки с дальнейшей механической очисткой последнего в другом помещении;
стерилизацию после механической очистки клеток и инвентаря, когда нет опасности наличия зараженного материала.
Независимо от размещения вивария (в отдельно стоящем здании или на верхнем этаже лабораторного корпуса) в дезинфекционно-моечном отделении следует предусматривать мусоропровод для удаления грязной подстилки и механизированный подъем материалов и оборудования.
Склад чистого инвентаря и оборудования размещается рядом с дезинфекционно-моечным отделением.
2.11. Для хранения подстилки (стружки, опилки, торф и др.) выделяются два помещения: одно для простерилизованной и упакованной в используемую данным виварием тару, другое - для хранения вновь приобретенной подстилки.
2.12. При проектировании помещений вивария необходимо обеспечить максимальную изоляцию:
всех его помещений от остальных подразделений, входящих в состав научно-исследовательского учреждения;
помещений изолятора и карантина от остальных помещений вивария;
между кормокухней, помещениями для животных и дезинфекционно-моечным отделением.
2.13. В каждом конкретном случае площадь, занимаемая кормокухней, дезинфекционно-моечным отделением и складом чистого запасного инвентаря, устанавливается в зависимости от применяемого оборудования, степени механизации производственных процессов и видов корма для подопытных животных.
Размеры площадей вышеперечисленных помещений указываются в задании на проектирование.
3. Ветеринарно-санитарные и технологические требования к строительным решениям помещений вивария и инженерному оборудованию
Светильники и осветительная арматура закрытого типа должны быть доступны для влажной очистки.
3.5. Помещения вивария, в которых содержатся лабораторные животные, оборудуются принудительной приточно-вытяжной системой вентиляции, обеспечивающей кратность воздухообмена и температурно-влажностный режим в соответствии с данными, приведенными в табл. .
|
Вид животных |
Температура, °С |
Относительная влажность, % |
Максимально допустимая концентрация в воздухе |
|||||
|
колебания |
средняя |
колебания |
средняя |
аммиака, мг/л |
углекислоты по объему, % |
вытяжка |
приток |
|
|
Мыши |
18 - 22 |
50 - 65 |
0,01 |
0,15 |
||||
|
Крысы |
18 - 22 |
50 - 65 |
0,01 |
0,15 |
||||
|
Хомяки |
18 - 22 |
50 - 65 |
0,01 |
0,15 |
||||
|
Морские свинки |
15 - 18 |
50 - 65 |
0,01 |
0,15 |
||||
|
Кролики |
15 - 18 |
50 - 65 |
0,01 |
0,15 |
||||
|
Собаки |
18 - 22 |
50 - 65 |
0,01 |
0,15 |
||||
|
Кошки |
18 - 22 |
50 - 65 |
0,01 |
0,15 |
||||
3.6. Температурно-влажностный режим в других помещениях вивария должен обеспечиваться в соответствии с данными, приведенными в табл. .
|
Помещение |
Температура в холодный и переходный период года, °С |
Кратность воздухообмена (объемов в час) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
приток |
вытяжка |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1. Для персонала |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2. Для приема животных |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
3. Для исследований |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
4. Моечное-стерилизационное |
1 - 2 |
2 - 3 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
5. Для усыпления (эвтаназии) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
6. Вскрывочное |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
7. Утилизационное |
По расчету |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
8. Для содержания подопытных сельскохозяйственных животных |
3.11. Для отвода и сбора сточных вод после мойки и дезинфекции технологического оборудования и полов следует предусматривать устройство лотков, перекрытых съемными дырчатыми плитами и трапами. Уклон лотков должен быть не менее 0,02. 3.12. При проектировании системы локальной канализации вивариев следует соблюдать следующие требования: сточные воды из помещений для сжигания трупов подлежат стерилизации в манжусах острым паром при температуре 120 °С в течение 30 мин или в пароструйной установке при температуре 110 °С в течение 10 мин; при наличии особо опасных инфекций сточные воды стерилизуют при 140° и 130 °С в течение 20 и 60 мин соответственно; производственно-бытовые стоки от мытья полов и мытья и дезинфекции технологического оборудования должны собираться в специальный приемник, а перед спуском в канализацию дезинфицироваться хлорсодержащими препаратами; ливневые стоки с территории отдельно стоящих вивариев, неблагополучных в ветеринарно-санитарном отношении, подлежат дезинфекции химическими препаратами; образующиеся механические и биологические осадки сточных вод подвергаются сжиганию. 3.13. Магистральные короба приточно-вытяжной вентиляции, электропитание, трубы водопровода и канализации должны располагаться в специальных нишах коридоров и иметь свободный доступ для проведения осмотра и ремонта. 3.14. Изолированные помещения для содержания подопытных животных, зараженных культурами возбудителей особо опасных инфекций или радиоактивными веществами, и помещение изолятора оборудуются локальными системами вентиляции с фильтрами, обеспечивающими 100 %-ную очистку и дезинфекцию выбрасываемого воздуха. Система вентиляции должна обеспечивать в этих помещениях пониженное (на 3 - 5 мм рт. ст.) давление атмосферного воздуха по отношению к другим помещениям вивария. Вентиляция в этих помещениях за счет открывания окон запрещена. 4. Оборудование вивария и условия размещения животных4.1. Мыши, крысы, хомяки, морские свинки и кролики размещаются в клетках, устанавливаемых на металлических стеллажах. 4.2. Настенные или другой конструкции стеллажи должны быть со съемными кронштейнами и подвижными полками, что позволяет переоборудовать их под клетки различных габаритных размеров с разными видами лабораторных животных. 4.3. Для расчета производственных площадей необходимо исходить из следующих нормативов размещения животных в клетках (табл. ).
Примечания. 1. Для примерного определения производственной площади следует исходить из расчета, что на 1 см 2 площади дна клетки должен приходиться 1 г массы животного. 2. Стеллажи размещаются в основном вдоль стен и должны занимать примерно 40 % производственной площади. 4.4. Собаки размещаются в отдельных кабинах (боксах) строго индивидуально. Размеры бокса должны соответствовать длине и росту животных. Размеры бокса для крупных собак живой массой свыше 22,5 кг - 1,2×1,8 м = 2,2 м 2 , средних массой 16 - 22,5 кг - 1,2×1,5 м = 1,8 м 2 , небольших массой 4,5 - 16 кг - 0,9×1,2 м = 1,1 м 2 . Зазор между прутьями 4,5 - 5,5 см, диаметр металлических прутьев 0,5 - 0,6 см. Боковые стенки - сплошные. На нижнюю стенку (пол) укладывают деревянные щиты. Кормление и поение - в боксе. Вольеры для выгула устраивают индивидуальные, из расчета до 2 м 2 на одно животное. Время выгула - не менее 2 раз в сутки, продолжительность - не менее 20 мин. Следует предусматривать раздельное секционное содержание самцов от самок, щенков и агрессивных животных. 4.5. На территории вивария для собак возводят специальные помещения, оборудованные кабинами. К кабинам пристраивают вольеры (выгулы). У каждой собаки должен быть свой вольер. Размеры кабины, м: длина - 2; ширина - 1,5; высота передней стенки - 2,5 и задней - 1,5 - 2; высота дверей кабины - 1,7, ширина - 0,7. Над дверью кабины устанавливают застекленную раму. Внизу двери, установленной в задней стенке кабины, являющейся передней стенкой вольера, делают лаз в вольер размерами 40×50 см, который на зиму завешивают плотной тканью для защиты от холода. Размеры вольера, м: длина - 3, ширина - 2, высота - 2,2. В его передней стенке делают дверь размерами 1,8×0,7 м. 4.6. Кошки размещаются в вольерах по пять голов, где предусматривается устройство полок (лежаков), достаточных по площади для размещения всех животных. Площадь вольера на одну кошку 0,5 м 2 . Перед входом в вольер оборудуется сетчатый тамбур. 4.7. В случае размещения в вивариях для научных целей сельскохозяйственных животных и птицы помещения для них сооружаются в соответствии с действующими нормами технологического проектирования с соблюдением зоогигиенических нормативов, изложенных в этих нормах. 5. Прием животных в виварий5.1. Пополнение вивария животными и птицей производится из специализированных питомников, благополучных по инфекционным заболеваниям. Приобретение животных и птиц в других организациях и у частных лиц допускается при отсутствии возможности закупки их в питомниках и наличия при каждой покупке ветеринарного свидетельства о благополучии организации (хозяйства, частного лица) по инфекционным заболеваниям. 5.2. Прием животных в виварий производится при наличии ветеринарного свидетельства или сопроводительных документов из питомника. 5.3. Полученные из питомника животные размещаются в изолированных секциях сроком на три дня для адаптации к новым условиям. Последующие сроки изоляции или карантина для этих животных определяются в зависимости от условий содержания животных, характера предстоящих экспериментов, расстояния, условий перевозки и др. 5.4. Для животных, полученных не из питомников, устанавливаются следующие сроки их карантина: для мышей и крыс - 14 дней, морских свинок и кроликов - 21, собак и кошек - 30, для остальных животных и птиц - 21 день. В отдельных случаях при использовании в экспериментах беременных самок, новорожденных и молодых животных, а также в краткосрочных опытах продолжительность карантина может быть сокращена при условии размещения этих животных в изолированных помещениях и соответствующего наблюдения. 5.5. В период карантина за животными ведется ежедневное клиническое наблюдение: термометрия и регистрация общего состояния животных в специальном журнале. 5.6. В карантинных и экспериментальных секциях животные помещаются в чистые, заранее продезинфицированные (проавтоклавированные) клетки. 5.7. Уход за животными, находящимися в здании карантина, осуществляется персоналом, закрепленным за данными помещениями. 5.8. Запрещается выносить из карантинных помещений в другие помещения и секции для экспериментальных животных корма, спецодежду и инвентарь. 5.9. В течение периода карантина производится периодическая смена клеток. По окончании карантина освободившиеся клетки и инвентарь передаются в дезинфекционно-моечное отделение. Чистка и мойка клеток и другого инвентаря из карантинных секций могут производиться в общем дезинфекционно-моечном отделении вивария только после предварительного обеззараживания. Отходы также должны обеззараживаться или сжигаться. Методы дезинфекции, дезинсекции и режим автоклавирования устанавливаются в каждом конкретном случае в зависимости от специфики работы учреждения. 5.10. В период адаптации или карантина животные с подозрением на инфекционные заболевания подвергаются бактериологическому исследованию. При подтверждении инфекционного заболевания мыши, крысы, хомяки, морские свинки и кролики всей поступившей партии уничтожаются, а в отношении собак, кошек и других животных сроки карантина продлеваются в зависимости от установленного заболевания. 5.11. Помещения карантина после каждой партии переданных на эксперимент животных и после каждого случая выявления инфекционных заболеваний подвергаются тщательной дезинфекции. 5.12. В случае возникновения массовых заболеваний среди животных, наблюдавшихся на карантине, или при обнаружении в период экспериментов отдельных случаев инфекционных заболеваний, особо опасных для лабораторных животных и человека, в виварии проводится необходимый комплекс профилактических мероприятий. В этом случае проведение опытов на животных временно прекращается. 5.13. По истечении срока карантина животные переводятся в экспериментальные секции. 6. Режим работы и основные правила содержания животных6.1. В каждом отдельном помещении рекомендуется содержать животных только одного вида. Если по условиям эксперимента необходимо совместное содержание лабораторных животных разных видов в одной секции, то их следует размещать на разных стеллажах. 6.2. На каждой клетке (боксе, вольере и т.д.) должна быть этикетка с указанием данных о животном и сроках эксперимента. 6.3. Лабораторные животные и птицы содержатся в клетках со сплошным дном на подстилке или в клетках с сетчатым дном - полом. В качестве подстилки применяются древесные опилки, стружка или подстилочный торф. Подстилка заранее автоклавируется или выдерживается в сухожаровом шкафу (при 150 - 180 °С 15 - 20 мин). Толщина слоя подстилки в клетке 5 - 10 мм. При содержании животных в клетках с сетчатым дном подстилка насыпается в поддон (противень), находящийся под сетчатым полом. 6.4. Вся работа по уходу и содержанию лабораторных животных строится в соответствии с распорядком дня и регламентом работ, утвержденными руководителем данного учреждения. В распорядке дня предусматривается время на санитарную обработку помещения и оборудования, раздачу кормов и проведение экспериментальных работ и манипуляций. 6.5. Кормление лабораторных животных осуществляется в соответствии с существующими нормами. 6.6. Корма и полуфабрикаты хранятся в специально отведенном для этой цели помещении. Выдача кормов производится в установленном порядке. В кормокухне вивария допускается хранение не более чем двух-трехдневного запаса кормов. При кормлении животных гранулированными кормами и при наличии в клетках бункеров-кормушек разрешается авансовое получение кормов со склада на семь-десять дней. 6.7. Для хранения запаса кормов на кормокухне и в кладовой вивария оборудуются специальные лари (металлические или обитые изнутри жестью). Скоропортящиеся продукты хранятся в холодильнике. Доставка кормов со склада производится специально выделенным персоналом (рабочими, не занятыми непосредственно уходом за животными). 6.8. Распределение кормов по комнатам-секциям производится специально выделенным для этих целей рабочим или персоналом кухни в продезинфицированной посуде (таре), закрепленной за каждой секцией. Списание кормов осуществляется в установленном порядке согласно фактическому наличию животных на каждый день. 6.9. Вход в кормокухню персонала, осуществляющего уход за лабораторными животными, и посторонних лиц запрещается. 6.10. Снабжение лабораторных животных питьевой водой производится из водопровода, качество воды должно соответствовать СаНПиН 2.1.4.1074-01 . 6.11. Проращивание зерна на зеленую массу для подкормки лабораторных животных производится в специально отведенных для этих целей помещениях. Допускается скармливание животным корневой массы растений при отсутствии в ней плесени. 6.12. Раздача кормов и поение животных должны осуществляться только после окончания уборки помещения, чистки или смены клеток и выноса из секций грязного оборудования, поддонов с подстилкой и других материалов, подлежащих дезинфекции или утилизации. 6.13. Чистка клеток и уборка комнат производится с помощью инвентаря, строго закрепленного за каждой комнатой. 6.14. При периодической смене клеток животные 1 - 2 раза в неделю пересаживаются в заранее продезинфицированные клетки с подготовленной подстилкой, кормушками и поилками. Грязные клетки вместе с подстилкой, кормушками и поилками передаются в дезинфекционно-моечное отделение для их последующей обработки. 6.15. Чистка клеток осуществляется ежедневно. При этом загрязненная подстилка и прочие отходы из клеток собираются в специальные металлические бачки с крышками. Бачки плотно закрываются и передаются в дезинфекционно-моечное отделение. 6.16. При использовании клеток с сетчатым дном и изолированными от клеток поддонами последние периодически (не реже одного раза в неделю) заменяются новыми. Грязные поддоны с подстилкой передаются в дезинфекционно-моечное отделение для их последующей обработки. 6.17. При обслуживании одним рабочим нескольких видов лабораторных животных сначала обрабатываются клетки с морскими свинками, затем клетки с мышами, крысами и кроликами, в последнюю очередь - помещения, где содержатся собаки и кошки. 6.18. Мыть и дезинфицировать клетки, кормушки и поилки непосредственно в секциях запрещается. 6.19. Перед окончанием рабочего дня в секциях, производится влажная уборка пола с использованием 1 %-ного раствора хлорамина или другого дезинфицирующего вещества. Не реже одного раза в месяц проводится санитарный день, в течение которого осуществляется уборка всех помещений. Порядок проведения санитарного дня определяется заведующим виварием. 6.20. Дезинфекция, чистка и мойка клеток, кормушек, поилок и другого инвентаря производится рабочими, специально закрепленными за дезинфекционно-моечным отделением. Контроль за эффективностью чистки и обеззараживания инвентаря возлагается на ветеринарного врача вивария. 6.21. Условия сбора, хранения, вывоза (или утилизации) отходов (подстилка, навоз, остатки корма и т.д.) должны быть определены в каждом конкретном случае по согласованию с местными органами и учреждениями Роспотребнадзора. При работе с инфицированным материалом необходимо проводить обезвреживание отходов с помощью автоклавирования или обработки дезинфицирующими растворами. 6.22. В секциях с подопытными животными следует вести постоянный контроль за температурно-влажностным режимом. Для контроля качества воздушной среды в помещениях, где содержатся животные, рекомендуется периодически (2 - 3 раза в месяц) определять концентрацию вредных газов (диоксида и аммиака). 6.23. Передача животных на опыты производится по разовым требованиям согласно годовой заявке от лабораторий, утвержденной руководителем учреждения. Работа с животными разрешается только в часы, предусмотренные распорядком дня вивария. 6.24. При обнаружении в секциях больных животных последние с ведома экспериментатора уничтожаются или переводятся в изолятор. Вопрос о дальнейшем использовании заболевших животных решается в течение не более двух суток. 6.25. Трупы животных до патологоанатомического вскрытия хранятся в специальном холодильнике не более одних суток, после чего подлежат утилизации. Хранение трупов животных в клетках и иа полу в экспериментальных секциях категорически запрещается. 6.26. Патологоанатомическое вскрытие животных производится экспериментатором. В случае гибели животного вне зависимости от эксперимента на вскрытии присутствует ветеринарный врач вивария. 6.27. Каждый случай падежа или вынужденного убоя животных должен быть зафиксирован в специальном журнале. 6.28. Запрещено посещение вивария посторонними лицами без специального разрешения. Сотрудники учреждения, выполняющие работы в виварии, обязаны: соблюдать установленные правила распорядка дня и режим работы вивария; вести систематические наблюдения за своими экспериментальными животным; вести первичную документацию, своевременно заполняя этикетки на клетках с экспериментальными животными; посещать только те помещения вивария, в которых находятся животные, закрепленные за данным сотрудником; по окончании экспериментов или любой другой текущей работы с подопытными животными оставлять рабочее место в надлежащем порядке; следить за своевременным списанием вышедших из опыта, павших или вынужденно убитых экспериментальных животных; сообщать специалистам вивария о всех замеченных случаях заболеваний экспериментальных животных, а также своевременно уведомлять специалистов вивария о предполагаемых патологических состояниях животных в соответствии с условиями эксперимента. 6.29. Сотрудникам учреждения, выполняющим работу в виварии с экспериментальными животными, запрещается давать какие-либо указания рабочим по изменению режима содержания и кормления животных без согласования со специалистами вивария. 6.30. При проведении сотрудниками данного учреждения совместных исследований на животных в других учреждениях запрещается на это время работа этих сотрудников в (клинике) виварии своего института (учреждения). 6.31. Все действия, которые могут причинить лабораторным животным боль (операции, тотальное обескровливание, вживление датчиков и т.д., а также вынужденный убой животных), должны производиться с использованием наркотизирующих средств. Если по условиям эксперимента противопоказано применение анестезии, то все вышеуказанные действия необходимо проводить в максимально короткий срок. 6.32. В ходе проведения эксперимента сотрудник, проводящий этот эксперимент, должен в обязательном порядке соблюдать следующие правила гуманного обращения с лабораторными (экспериментальными) животными. В случаях, когда предполагается хирургическое вмешательство или проведение эксперимента с болевым раздражением, анестезия должна проводиться до привязывания животного к станку. Расчет количества анестезирующего вещества должен проводиться на 1 кг или 1 г массы животного. Название вещества и его количество необходимо фиксировать не только в протоколе опыта, но и специальной карте. В ходе эксперимента, когда он оказывается более длительным, чем рассчитывалось первоначально, обязательно проводится добавочное введение анестезирующих веществ. Если острый опыт должен закончиться гибелью животного, то экспериментатор обязан умертвить животное до окончания действия анестезирующего вещества. После окончания хирургического вмешательства животное должно быть перенесено в послеоперационное помещение на специальных носилках, исключающих возможность смещения тканей, расхождения швов и т.д. Экспериментатор должен предусмотреть возможность появления болевых ощущений у животного в послеоперационном периоде и назначить обезболивающие препараты. 7. Штатная численность обслуживающего персонала вивария7.1. Штатная численность обслуживающего персонала вивария определяется в зависимости от объема и характера экспериментальных исследований, а также от количества лабораторных животных. При этом необходимо исходить из следующих норм нагрузки животных одного вида на одного рабочего по уходу (с учетом норм размещения животных в клетках).
При обслуживании одним человеком животных нескольких видов расчет проводится, исходя из приведенных выше норм. В каждом конкретном случае при установлении норм нагрузки по уходу за животными на одного рабочего необходимо учитывать тип клеток, степень механизации производственных процессов, тип кормления (натуральные корма или гранулированные), периодичность, характер и особенности проводимых исследований и т.д. 7.2. При работе с радиоактивными веществами или особо опасными инфекциями, а также при содержании видов животных, не указанных в табл. , нормы обслуживания устанавливаются руководителем научного учреждения на основе хронометража отдельных операций и с учетом действующих нормативов по обслуживанию сельскохозяйственных животных. 8. Правила личной гигиены сотрудников вивария8.1. Персонал вивария должен быть обеспечен спецодеждой, спецобувью, мылом и полотенцами в соответствии с действующими нормативами. 8.2. В комнатах с животными, кормокухне, дезинфекционно-моечном отделении необходимо иметь дезинфицирующие растворы для обеззараживания рук. 8.3. Персонал вивария обязан: перед началом работы снять верхнюю одежду, обувь, надеть спецодежду, спецобувь; по окончании работы (желательно и до начала работы) пройти обработку в санитарном блоке (принять душ или ванну); вешать домашнюю одежду и спецодежду только в разных отделениях индивидуального шкафа; периодически (но не реже одного раза в месяц) дезинфицировать свои индивидуальные шкафы; по окончании каждого отдельного этапа работы в соответствии с распорядком дня, а также перед приемом пищи обязательно мыть и дезинфицировать руки. 8.4. В производственных помещениях вивария категорически запрещается принимать пищу и курить. 8.5. Вновь принятые на работу с лабораторными животными лица должны пройти медицинское обследование, включающее в себя исследования на наличие возбудителей туберкулеза и всей группы кишечных инфекций. Последующие обследования проводятся не реже одного раза в год. Больные туберкулезом, венерическими, кожными и другими заразными заболеваниями к работе в виварии не допускаются. 8.6. При проведении на животных экспериментов с инфекционными возбудителями, опасными для людей, обслуживающий персонал вивария подвергается профилактической иммунизации. |
Метод фиксации |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Крупный рогатый скот |
Животного укрощают путем сдавливания носовой перегородки пальцами, щипцами Гармса, Николаева, носовыми кольцами или ограничивают движения, удерживая его за рога с помощью веревки, за шею, голову и второй петли вокруг носа. Задние конечности фиксируют веревочной петлей, которую накладывают на обе конечности несколько выше скакательных суставов. При расчистке и обрезке копыт на тазовые конечности животных можно наложить закрутку на голень. Быков фиксируют с помощью носовых колец и прочного ремня-ошейника с цепью. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Быков-производителей независимо от их нрава доставляют на обследование только на недоуздке и обязательно применяют палку-водило (карабин) длиной около 2 м, которую прицепляют за носовое кольцо, что предупреждает внезапное нападение животного на человека. Телят удерживают руками за шею, уши или с помощью шейной глухой петли со специальным узлом и привязывают веревкой к стойке. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Свиньи |
Животных фиксируют в стоячем положении путем захвата верхней челюсти металлическим тросом и ручкодержателем или в станке несложной конструкции. Откормочный молодняк и подсвинков удобно удерживать щипцами, предложенными К.П. Соловьевым. При работе с хряками, старыми боровами и кормящими свиноматками, особенно фиксированными в станках, требуется осторожность. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Козы и овцы |
Животных удерживают за рога или шею. В необходимых случаях фиксируют в лежачем положении на столе. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Лошади |
Лошадей фиксируют так, чтобы они не могли ударить передними и задними конечностями, укусить. К лошадям следует подходить несколько сбоку, в направлении плеча и лопатки, лучше с левой стороны, поскольку лошадь привыкает к этому в процессе эксплуатации. Подходят к голове, левой рукой берут за недоуздок, уздечку или гриву, а правой - поглаживают и похлопывают по шее, холке, затем по лопатке и плечу. Если животное содержится без привязи в деннике, то его следует окликнуть, чтобы привлечь внимание к себе, подозвать, произнося ласковые слова. Необходимо, чтобы лошадь обязательно встала головой к человеку. К находящемуся в станке или на коновязи животному следует подходить не сзади, а несколько сбоку с той стороны, куда оно смотрит. При термометрии, ректальном исследовании, проведении различных лечебных манипуляций с целью обеспечения безопасности работы ветеринарного специалиста необходимо поднять грудную конечность с той стороны, с которой манипулирует специалист, или наложить путки на одну или обе задние конечности. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Грудную конечность фиксируют, подняв за щетку или путовую часть и согнув в запястном суставе. При этом встают сбоку от животного спиной к его голове. Поднятую конечность удерживают двумя руками, а при длительных манипуляциях - с помощью путки или веревки, перекинутой через спину. Нельзя класть поднятую конечность животного на свое колено, так как у животного появляется четвертая точка опоры, что небезопасно для человека. Не следует привязывать веревку к какому-либо предмету или обматывать вокруг туловища животного, так как при неожиданном падении лошадь не сможет быстро высвободить конечность. При обследовании задних частей тела фиксируют тазовую конечность. Встав у крупа лошади лицом к хвосту, одной рукой опираются в маклок, а другой легко похлопывают по ноге сверху вниз, поднимают ее, застегивают путовый ремень или надевают веревочную петлю, которую затем пропускают между передними конечностями, обводят вокруг шеи и завязывают нестягивающейся петлей. При исследовании строптивых и для укрощения беспокойных лошадей применяют закрутки и губные клещи. Чтобы наложить закрутку, надо ввести кисть руки в петлю закрутки. Захватить верхнюю губу, оттянуть ее вперед, левой рукой переместить петлю закрутки на губу и туго закрутить. Животных можно надежно фиксировать в специальных станках. В станке лошадь рекомендуется привязывать на растяжку, а строптивому животному, чтобы оно не завалилось, под живот подвести ремни. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Верблюды |
Верблюды доставляются для исследований на недоуздке. Подходить к верблюдам надо осторожно, лучше сбоку (со стороны грудных конечностей). Способы укрощения этих животных такие же, как крупного рогатого скота и лошадей. Следует учитывать специфические особенности поведения этих животных. Желательно, чтобы для фиксации верблюдов привлекался персонал, постоянно ухаживающий за ними. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Птица |
Птицу фиксируют, удерживая в естественном положении за конечности и крылья, не сдавливая грудную клетку, чтобы избежать удушья. При работе с водоплавающими (гуси, утки) нужно удерживать и голову, чтобы избежать удара в глаз, а манипуляции проводить на расстоянии вытянутых рук. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Пушные звери |
Зверей удерживают специальными щипцами или руками в брезентовых (с ватной подкладкой) рукавицах. Кладут на стол и держат одной рукой за шею, другой - за туловище. Ротовую полость можно раскрыть с помощью зевников конструкции В.Л. Берестова, рекомендуется использовать специальные намордники. Можно фиксировать животных в сетчатых ловушках, применять анальгезирующие или транквилизирующие средства с местно-анестезирующими веществами, а также средство для наркоза. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Собаки |
При помощи хозяина на животных надевают намордник или завязывают им ротовую полость крепкой тесьмой. С этой целью на челюсти сверху накладывают тесьму, завязывают простым узлом под нижней челюстью, затем окончательно закрепляют на затылке морским узлом. При подозрении на бешенство, а также злых и беспокойных собак лучше поместить в специальную металлическую клетку, одна сторона которой передвигается и зажимает ее. Для фиксации собак в лежачем положении используют операционный стол для мелких животных, позволяющий придать им любое удобное для работы положение. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Кошки |
При болезненных манипуляциях животных фиксируют в специальном матерчатом рукаве или обертывают полотенцем, оставляя свободной часть тела, подлежащую исследованию. Морду можно завязать, как собаке, а ноги зафиксировать руками, надев кожаные или резиновые перчатки. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
СНиП 11.01-2003. Инструкция о порядке разработки, согласования, утверждения и состава проектной документации на строительство предприятий, зданий и сооружений.
. СаНПиН 2.2.1/2.1.1.1200-03 . Санитарно-защитные зоны и санитарная классификация предприятий, сооружений и других объектов (Новая редакция. Утверждена постановлением Главного санитарного врача РФ № 74 от 25.09.07, зарегистрирована Министерством юстиции РФ № 10995 от 25.01.08).
Питьевая вода. Гигиенические требования к качеству воды централизованных систем питьевого водоснабжения. Контроль качества.
Немаловажное значение для токсикологического эксперимента имеют условия содержания подопытных животных. Содержание животных в условиях, вызывающих у них стресс (одиночное содержание в пенале, грубая фиксация в нефизиологическом положении), приводит к увеличению токсичности. Изменения в питании также сказываются на показателях токсичности.
Для экспериментальных исследований в токсикологических лабораториях используют крыс линии Вистар или белых беспородных крыс, которые являются альбиносами черной (Rattus rattus) и серой (пасюк - Rattus norvegicus) крыс, а также белых мышей, которые являются альбиносами домовой мыши (Mus musculus). И крысы, и мыши принадлежат к одному и тому же отряду грызунов (Rodentia), семейству мышиных (Muridae).
Важное преимущество белых крыс как лабораторных животных заключается в том, что они довольно устойчивы к инфекционным заболеваниям и дают большой приплод.
Белых крыс содержат в помещениях с хорошей вентиляцией, достаточным освещением и равномерной температурой - 20- 22 *С. Лабораторные крысы плохо переносят холод. Влажность воздуха в помещениях не должна превышать 40-45 %.
В качестве подстилки для животных используют крупные опилки, измельченный торф или сечку из соломы или бумаги, тряпки. В клетках поддерживают надлежащую чистоту. Они должны быть всегда сухими, чистыми, хорошо вентилируемыми. Не допускают скопления в них мочи и фекалий.
Кроме ежедневной уборки клетки I -2 раза в месяц тщательно моют и дезинфицируют. Дезинфицировать клетки лучше всего крутым кипятком, горячим 5-10%-м раствором едкой щелочи или такими противомикробными средствами, как хлорная известь, креолин, сулема, формалин и др.
Крысы - всеядные животные, поэтому нельзя ограничивать их рацион только растительной пищей. Крысы, не получающие в необходимых количествах продукты животного происхождения (молоко, мясо, мясокостную муку), минеральные вещества и витамины, перестают расти.
Суточная потребность взрослой крысы в кормах составляет в среднем 30-32 г, из них 25 г смешанного корма и 5-7 г овощей.
Кормят крыс обычно 2 раза в сутки. Ввиду того что крысы ночные животные и едят в темное время суток, основную часть корма следует давать вечером, примерно к 20 ч. Не рекомендуется резко менять пищевой режим, к новой пище крыс нужно приучать постепенно. Вода для питья должна быть чистой и свежей, рекомендуется пользоваться кипяченой водой. Заменять воду молоком также надо постепенно, в противном случае животные отказываются от еды и заболевают.
что мыши более чувствительны к нарушениям температурного ре жима, смене корма и инфекционным заболеваниям (в частности сальмонеллезу). У мышей в гораздо большей степени, чем у крыс проявляется «социальная» иерархия в группе - борьба за лидерство, вследствие чего не рекомендуется изменять состав мышей Е клетках.
Суточная потребность взрослой мыши в кормах составляет Е среднем 9,5-10 г смешанного корма и 1-2 г овощей.
ИСПОЛЬЗОВАНИЕ ЛАБОРАТОРНЫХ ЖИВОТНЫХ
В ТОКСИКОЛОГИЧЕСКОМ ЭКСПЕРИМЕНТЕ
В методических рекомендациях проанализированы возможности использования различных видов лабораторных животных в токсикологических экспериментах, представлены основные типы токсикологических исследований и способы введения химических веществ при их осуществлении; приведены варианты моделирования алкогольной интоксикации; обоснованы принципы моделирования комбинированного воздействия хронической алкогольной интоксикации и алиментарной недостаточности.
Методическое пособие составлено,
К.В. Шелыгиным, д.б.н.
И.А. Кирпич, доц.
В.Я. Леонтьевым, проф.
А.Г. Соловьевым.
под редакцией проф., академика РАМН П.И. Сидорова.
Рецензент: зав. кафедрой биологии и экологи человека и животных Поморского государственного университета им. Ломоносова, д.б.н., проф. В.А. Барашков
1. Моделирование острых и хронических токсических эффектов– важное направление клинической токсикологии
2. Основные лабораторные животные, используемые в токсикологических исследованиях
2.1 Грызуны
2.3. Крупные млекопитающие
3. Острые, подострые и хронические эксперименты в токсикологии
4. Способы введения токсических веществ
5. Моделирование острой и хронической алкогольной интоксикации
6. Моделирование комбинированного воздействия хронической алкогольной интоксикации и алиментарной недостаточности
Литература
1. МОДЕЛИРОВАНИЕ ОСТРЫХ И ХРОНИЧЕСКИХ ТОКСИЧЕСКИХ
ЭФФЕКТОВ – ВАЖНОЕ НАПРАВЛЕНИЕ КЛИНИЧЕСКОЙ ТОКСИКОЛОГИИ
Одно из основных направлений современной токсикологии напрямую связано с исследованием патологических изменений организма при острых и хронических токсических воздействиях.
Большую помощь в изучении механизмов развития морфофункциональных осложнений острой и хронической интоксикации могут оказать эксперименты на лабораторных животных, поскольку прямые исследования не всегда возможны, а порой и этически недопустимы. Разумеется, экстраполяция экспериментальных данных на патологию человека в рамках развития положений клинической токсикологии требует определенной осторожности ввиду известных особенностей протекания метаболических процессов у животных, функциональных характеристик их внутренних органов, а подчас и существенных отличий в строении организма. Тем не менее, опыты на животных позволяют проследить динамику патологических изменений в органах и составить представление о развитии патологических процессов на системном, органном, клеточном и субклеточном уровнях, что является необходимым условием для разработки эффективных методов профилактики и лечения отравлений различной этиологии.
При проведении эксперимента необходимо руководствоваться принципами гуманного отношения к животным в соответствии с Международными рекомендациями (1993), а так же с соблюдением биоэтических норм и требований Международного комитета по науке (1978).
В соответствии с диффиренцированными задачами моделирования эффектов токсического воздействия химических соединений эксперименты могут проводиться на различных лабораторных животных, наиболее распространенными видами среди которых в токсикологических исследованиях являются грызуны, птицы и крупные млекопитающие.
2. ОСНОВНЫЕ ЛАБОРАТОРНЫЕ ЖИВОТНЫЕ,
ИСПОЛЬЗУЕМЫЕ В ТОКСИКОЛОГИЧЕСКИХ ИССЛЕДОВАНИЯХ
2.1. Грызуны.
При моделировании токсических эффектов химических веществ наиболее часто используются грызуны (мыши, крысы, морские свинки, кролики).
Белые лабораторные мыши, являющиеся альбиносами домашней серой мыши, используются для определения токсичности химических веществ, стандартизации фармакологических препаратов.
Морские свинки являются классическим объектом для изучения аллергогенности химических веществ, а так же проявлений авитаминозов. Изолированные органы этих животных применяются в фармакологических исследованиях.
Кролики в связи с особенностями протекания у них овуляторного цикла и высокой скоростью размножения удобны для выявления воздействия токсических веществ на репродуктивные функции.
Лабораторные крысы (альбиносы черной и серой крыс) являются наиболее распространенным видом экспериментальных животных для разработки моделей последствий острых и хронических интоксикации. В настоящее время выведено более 100 отдельных аутобредных стоков и инбредных линий лабораторных крыс. Наиболее часто при токсикологических исследованиях используются крысы стоков Wistar, Bio Breeding Sprague-Dawley, C57BL, CFI, C3H и др. Отдельно выделяют конвенциональных (беспородных) животных, микрофлора которых полностью или частично неизвестна.
Удобство использования крыс для исследования токсических эффектов химических и биологических препаратов объясняется простотой их содержания, возможностью размещения на сравнительно небольшой территории достаточного количества животных, небольшим весом, устойчивостью к инфекционным заболеваниям, большим приплодом, который они дают. Крыс легко фиксировать рукой; постоянная заполненность желудка пищей при обычном режиме питания позволяет вводить им интрагастрально достаточные дозы токсических агентов, не вызывая катаральных изменений слизистой. Предпочтение в токсикологических исследованиях отдается самцам, так как они не имеют гормональных колебаний, способных оказывать влияние на мембранотропное действие ядов; целесообразнее использование молодых животных, поскольку у них меньше толерантность к различным токсическим веществам.
Наиболее часто при проведении токсикологических экспериментов используются куры, утки, гуси, индейки. Отдельно выделяют птиц - свободных от специфических патогенных микроорганизмов (specific pathogen free - SPF).
Птицы являются удобной моделью для проведения исследований влияния химических веществ на метаболические процессы, поскольку они протекают более интенсивно и быстрее, чем у других животных. Однако, при проведении исследований необходимо учитывать некоторые анатомо-физиологические особенности строения организма птиц. Так, например, у последних нет потовых и сальных желез, а так же мочевого пузыря, что имеет существенное значение для определения клиренса выведения токсических агентов и их метаболитов. Состав крови и мочи птиц существенно отличается от соответствующих физиологических показателей других животных. В отличие от млекопитающих птицы имеют особенности в строении желудочно-кишечного тракта, у них по-другому протекают процессы переваривания корма. В исследованиях на птицах удовлетворительным критерием является изменение массы тела.
При исследовании влияния токсических веществ на поведенческую активность необходимо учитывать, что реактивность птиц зависит от принадлежности их к яйценоской или мясной направленности, а также от степени их продуктивности.
При недостаточном освещении птицы не подходят к кормушкам и поилкам, поэтому, если по условиям эксперимента необходимо повысить потребление корма или жидкости, которые содержат токсическое вещество, используется искусственное освещение. Содержать птиц при проведении эксперимента рекомендуется группами, поскольку в этом случае они достигают большей массы и более резистентны к инфекциям.
2.3. Крупные млекопитающие.
Проведение токсикологических исследований на крупных млекопитающих (собаках, кошках, обезьянах) обусловлено наибольшей схожестью строения и функционирования их внутренних органов и систем, а также метаболических процессов с таковыми у человека.
Обезьяны, несмотря на сложность их содержания, используются в токсикологической практике при изучении влияния химических веществ на функции центральной нервной системы.
Кошки, как объект исследования чаще всего применяются в острых токсикологических экспериментах. Кроме того, их изолированные органы задействуют в целях выявления физиологических изменений при действии химических веществ.
Одним из часто используемых в клинической токсикологии крупных млекопитающих животных являются собаки. Для проведения токсикологических экспериментов наиболее пригодными считаются беспородные короткошерстные собаки со средней массой тела 10-15 кг, поскольку чистопородные и линейные животные более прихотливы в содержании и гораздо нестойки в хронических опытах. Оптимальный возраст животных 1,5-5 лет. Известно, что основные морфофункциональные изменения у собак при проведении токсикологических исследований во многом соответствуют таковым у человека.
В условиях проведения эксперимента необходимо учитывать, что собаки являются стайными животными с развитой иерархической системой, половыми и индивидуальными различиями темперамента, поэтому рекомендуется одиночное размещение собак в отдельных боксах. Собаки достаточно легко обучаются, что можно использовать при проведении некоторых процедур, ограничивая применение средств фиксации.
Кормление животных осуществляется согласно разработанным рационам и с учетом задач эксперимента. Однако, необходимо помнить, что желудочно-кишечный тракт собак не приспособлен к перевариванию большого количества растительной пищи.
3. ОСТРЫЕ, ПОДОСТРЫЕ И ХРОНИЧЕСКИЕ ЭКСПЕРИМЕНТЫ В ТОКСИКОЛОГИИ
Выбор продолжительности эксперимента при изучении токсических свойств изучаемых веществ определяется целями исследования (таблица 1).
Острый токсикологический эксперимент используется для моделирования острой токсичности вещества, проявляющейся после его однократного или повторного введения через короткие (не более 6 часов) интервалы в течение суток. Целями изучения острой токсичности являются определение безвредных, токсических, летальных доз вещества, его способности к кумуляции, а также причин гибели животных.
Подострый эксперимент проводится для определения допустимых условий воздействия, оптимальных суточных доз, для выбора доз в хроническом эксперименте.
Исследование токсических свойств веществ в субхроническом и хроническом экспериментах осуществляется с целью установления степени их повреждающего действия при длительном введении, определения уровня обратимости вызываемых ими повреждений, а так же выявления наиболее чувствительных к токсическому действию органов и систем организма.
|
Таблица 1 Продолжительность и цели токсикологического эксперимента |
||
|
Характер эксперимента |
Продолжительность |
Цели эксперимента |
|
|
Однократное введение; |
Определение смертельных доз, среднего времени гибели, порога острого действия химических веществ |
|
Подострый |
2-8 недель |
Определение кумуляции, аллергического действия, влияния на репродуктивную функцию химических веществ |
|
Субхронический |
13-18 недель |
Определение пороговой дозы общетоксического действия при установлении ПДК веществ в воздухе |
|
Хронический |
6-12 месяцев |
Определение пороговой дозы общетоксического действия при установлении ПДК веществ в воде и пище |
|
Пожизненный |
от 1 года и более |
Определение пороговой дозы общетоксического действия химических веществ |
4. СПОСОБЫ ВВЕДЕНИЯ ТОКСИЧЕСКИХ ВЕЩЕСТВ
Для формирования характерных токсически обусловленных патологических изменений у животных используются добровольные, полудобровольные и принудительные способы введения токсических веществ.
На добровольный выбор животными потребляемых жидкостей или сухих кормов влияют индивидуальная чувствительность, скорость метаболизма вещества, порода, возраст, условия содержания, наличие дополнительных стрессорных факторов, концентрация раствора, наличие пищевых добавок и т.д. Данный способ не может обеспечить достаточно высоких и стабильных доз поступления токсических веществ в организм, поэтому более эффективными являются модели полудобровольного и принудительного введения.
При полудобровольном способе животные имеют возможность самостоятельно регулировать количество потребляемого вещества. К ним, в частности, относится методика предоставления раствора исследуемого вещества в качестве единственного источника жидкости.
Способы принудительного введения позволяют обеспечить массивную токсическую нагрузку, что обусловливает высокую концентрацию агента в крови и приводит к быстрому развитию патологических изменений.
При изучении токсически обусловленной патологии особое значение придается способам, характеризующимся моделированием тех концентраций токсических веществ, которые встречаются в реальных условиях. Этим параметрам, например, соответствует способ интрагастрального введения этанола, при котором средние дозы спирта, получаемые животными на протяжении эксперимента, составляют, обычно, 4-10 г/кг в сутки.
Ингаляционный метод введения веществ позволяет создавать практически любые токсические нагрузки. В то же время, принудительная продувка токсических веществ через затравочную камеру требует значительного расхода химических ингредиентов, а постоянную их концентрацию создать, практически, невозможно. Существующий способ разлива химического вещества в камере, где находятся животные, более пригоден для моделирования острых отравлений, однако, при данном способе невозможен количественный токсикологический контроль в условиях работы с несколькими веществами одновременно.
Наиболее рациональным при использовании способа ингаляционного введения, является тот, при котором для принудительной продувки через затравочную камеру используется только чистый воздух. Исследуемые вещества при этом расположены внутри камеры в небольших сосудах, площадь открытого участка которых подбирается расчетным образом. Заменяя сосуды на более узкие или широкие, можно варьировать скорость испарения химических соединений, количество которых берется с таким учетом, чтобы по окончанию затравки какое-то содержимое их осталось в сосудах. Данный способ прост в применении, обладает высокой чувствительностью, позволяет точно создавать постоянную концентрацию, значительно экономить используемые химические вещества.
Выбор концентраций и доз химического соединения решается с учетом целей эксперимента и физиологических особенностей подопытных животных. Необходимо помнить, что количество вводимых растворов ограничивается рамками физиологических возможностей, массой и возрастом животных. Так, максимальные объемы введения у крыс составляют интраназально до 0,4 мл, ректально – 1 мл, внутрикожно – 0,04 мл, подкожно – 10 мл, внутримышечно и внутрибрюшинно – до 5 мл, внутривенно – 6 мл, внутрисердечно – 1 мл, субокципитально – 0,15 мл, интрагастрально при весе тела 100-190 г – 3 мл, 200-290 г – 4-5 мл, 250-300 г – 6 мл, 300 г и более – 8 мл. Максимальные объемы веществ у собак составляют при интраназальном введении – 4 мл, подкожном – 20 мл, внутримышечном – 12 мл, внутрибрюшинном – 20 мл.
В то же время, введение веществ животным производится с учетом особенностей их анатомии, а так же формы исследуемого вещества. Например, порошкообразные - вводятся крысам перорально, путем приготовления пилюль из данного вещества и муки, хлеба или его добавления к воде или корму.
Введение растворов веществ осуществляется перорально с помощью резинового или металлического зонда, интраназально с помощью мочевого катетера, ректально. Кожное введение подразумевает предварительное удаление волосяного покрова, выполнение насечек, после чего наносят исследуемое вещество. Внутрикожные инъекции осуществляют в задней части спины или на животе, предварительно так же удалив волосяной покров. Подкожные инъекции делают на шее, спине или животе. Внутримышечно вещества вводят в заднебедренные мышцы. Внутрибрюшинные инъекции выполняют в левый нижний квадрант брюшной полости. Внутривенно вещества вводят в хвостовую вену или в дорсальную вену полового члена. Введение веществ также возможно непосредственно в сердце, либо субокципитально предварительно анестезированной крысы.
Введение токсических веществ птицам осуществляется интрагастрально при помощи зонда, внутривенно в локтевую или плечевую вену крыла, внутрибрюшинно в правый нижний квадрант брюшной полости, подкожно через кожу на животе или внутримышечно через четырехглавую мышцу бедра.
Введение исследуемых веществ собакам выполняется путем их подмешивания к корму, питьевой воде, либо принудительно, когда вещество в виде таблетки кладется на спинку языка животного. Жидкие вещества, а так же растворы вводят при помощи ложки или спринцовки, однако более удобно использовать желудочный зонд. Кроме того, введение жидких веществ возможно интраназально с помощью катетера, ректально, подкожно в области спины, бедра или затылка, внутрикожно, накожно, внутримышечно – в мышцы бедра, внутривенно – в вены голени, стопы, предплечья, внутрибрюшинно. Существуют способы субокципитального, внутримозгового и внутрисердечного введения веществ, однако, их выполнение сопряжено с техническими трудностями и подвергает повышенной угрозе жизнь животного.
Для снижения трудностей, возникающих при экспериментальном изучении токсических свойств веществ, проявляющихся в необъективности подбора доз, их вариабельности, используется метод экспериментального изучения токсичности малотоксичных соединений, путем введения доз, соответствующих максимально возможному разведению химических соединений в известных максимально вводимых объемах, .позволяет быстро подобрать максимальную вводимую дозу на кг (г) веса животного, подтвердить или опровергнуть низкую токсичность изучаемых веществ, сравнить результаты различных исследователей между собой.
5. МОДЕЛИРОВАНИЕ ОСТРОЙ И ХРОНИЧЕСКОЙ АЛКОГОЛЬНОЙ ИНТОКСИКАЦИИ
Социологические исследования, проведенные в последние десятилетия, показывают стабильно высокий уровень распространенности как злоупотребления алкоголем, так и алкоголизма и его осложнений среди различных групп населения. В то же время, при проведении эпидемиологических исследований влияние множества социальных факторов не позволяет до конца выявить искомые зависимости течения различных проявлений алкоголизма. Поэтому одним из способов исследования алкогольобусловленной патологии в клинической наркологии является моделирование проявлений острой и хронической алкогольной интоксикации на лабораторных животных.
При моделировании острой алкогольной интоксикации используются максимально переносимые дозы этанола. В этом случае исследуются патологические изменения, сопровождающие развитие острого отравления вплоть до коматозного состояния.
Моделирование хронической алкогольной интоксикации позволяет получить характерные патологические изменения, сравнимые с таковыми у человека при длительном злоупотреблении алкоголем. При применении методик с длительным введением алкоголя необходимо учитывать возрастной фактор, так как скорость элиминации этанола из организма с постарением животных замедляется.
Средние дозы этилового спирта, получаемые животными на протяжении хронического эксперимента, зависят от его задач и составляют, например, для крыс - от 4-10 г на кг веса в сутки, но иногда используются и максимально переносимые дозы – до 15 – 20 г/кг. Наиболее адекватной для моделирования характерных проявлений алкогольной висцеропатологии на крысах, являются дозы в пределах 7 г/кг/сут. 40% этанола, соответствующие, в частности, ? DL50, что обусловливает в процессе хронической интоксикации достаточно быстрое развитие типичных алкогольных поражений внутренних органов, но не сопровождается массовой гибелью животных. Продолжительность хронического эксперимента колеблется от 5 суток до 4 лет также в зависимости от целей исследования.
6. МОДЕЛИРОВАНИЕ КОМБИНИРОВАННОГО ВОЗДЕЙСТВИЯ ХРОНИЧЕСКОЙ АЛКОГОЛЬНОЙ ИНТОКСИКАЦИИ И АЛИМЕНТАРНОЙ НЕДОСТАТОЧНОСТИ
Ряд клинических синдромов алкоголизма связывается с нарушением питания (в частности, обмена витаминов и белков) и изменением нутриентного статуса организма. Это обусловлено тем, что продолжительная алкогольная интоксикация в ряде случаев сопровождается недостаточностью питания, нарушением всасывания и метаболизма незаменимых факторов питания.
Ввиду того, что этанол, помимо высокой калорийности, не представляет пищевой ценности, при систематическом употреблении алкогольных напитков структура пищевого рациона претерпевает резкий дисбаланс, при этом часто наблюдается алиментарный дефицит, подобный дефициту при голодании. Нарушение обмена белков и общая белковая недостаточность при хронической алкогольной интоксикации достаточно обоснованно расцениваются как одни из типичных для рассматриваемой патологии проявлений. Недостаток отдельных факторов белкового питания может вызвать существенные нарушения обмена витаминов, что, в свою очередь, приводит к ухудшению функциональной активности внутренних органов. Поскольку некоторые из витаминов оказывают избирательное действие на отдельные их функции, хроническая алкоголизация еще более углубляет эти нарушения. Кроме того, при одновременном дефиците витаминов и белка морфофункциональные параметры могут отличаться от соответствующих характеристик изолированных форм алиментарной недостаточности.
На основании вышеизложенных данных, нами предложена модель комплексного воздействия хронической алкогольной интоксикации и алиментарной недостаточности - витаминов группы В, играющих важную роль при алкогольобусловленной патологии, и белка.
Алгоритм создания модели.
Алгоритм создания экспериментальной модели хронической алкогольной интоксикации на фоне алиментарного дисбаланса включает следующие компоненты:
1.Выбор лабораторных животных и условий их содержания
2. Выбор экспериментальных диет, необходимых дозировок этанола, способа его введения и продолжительности эксперимента
3.Оценка степени тяжести токсического воздействия.
Выбор лабораторных животных и условий их содержания
В качестве подопытных животных при моделировании длительной алкоголизации на фоне алиментарного дисбаланса при прочих равных условиях предпочтительнее использовать крыс. Выбор данного вида лабораторных животных обусловлен сравнимостью алкогольобусловленных изменений у крыс с таковыми у человека, морфофизиологическими особенностями этих животных (отсутствием отвращения к этанолу и рвотного рефлекса на его действие, постоянной заполненностью желудка пищей), простотой содержания и легкостью выполнения с ними различных процедур (фиксации, введения растворов веществ с помощью зонда и т. д.).
Животные должны содержаться в стандартных условиях вивария, иметь свободный доступ к пище и воде. Учитывая возможность поступления витаминов при копрофагии, крыс содержат в клетках с дном из крупноячеистой сетки.
Выбор экспериментальных диет, необходимых дозировок этанола, способа его введения и продолжительности эксперимента
Для наиболее полного изучения комплексного воздействия недостаточности витаминов группы В и белка животных рекомендуется разделить на четыре рабочие группы, получающие:
I – сниженное содержание витаминов группы В
II – сниженное содержание белка
III – сниженное содержание белка и витаминов группы В
IV – контрольная – содержится на обычном рационе вивария.
Например, рацион, практически исключающий содержание витамина В6 содержит 18-20% казеина, очищенного от витаминов, 73-71% сахарозы, 4% солевой смеси, 3% подсолнечного масла с 0,2% рыбьего жира.
При проведении эксперимента, в цели которого входит моделирование недостаточности определенных витаминов, следует максимально точно обеспечивать покрытие потребностей животных в других витаминах (таблица 2).
|
Таблица 2 Суточные дозы витаминов, покрывающие основные потребности крыс (по Ю.М. Островскому, 1979). |
|
|
Суточная доза, мкг |
|
|
Пантотенат | |
|
Пиридоксин | |
|
Витамин С | |
|
Токоферол | |
В связи с изменением массы тела животных рационы необходимо корректировать в соответствии с приказом МЗ РСФСР №1179 от 10. 10. 1983 «Об утверждении нормативов затрат кормов для лабораторных животных в учреждениях здравоохранения».
Моделирование недостаточности в рационе белка осуществляется путем содержания лабораторных животных на специализированных диетах, составленных по методике А.А. Покровского с соавт. (1974).
Наиболее приемлемой в условиях хронического эксперимента на крысах является экспериментальный рацион, содержание белка в котором в 4,6 раза меньше, чем при стандартном кормлении (таблица 3).
|
Таблица 3 Суточный рацион крыс с пониженным содержанием белка (по А.А. Покровскому, 1974) |
||
|
Ингредиенты |
% по калорийности |
|
|
Казеин пищевой | ||
|
Смесь лярда и подсолнечного масла 1:1 | ||
|
Крахмал маисовый | ||
Для достижения равной калорийности между стандартным и экспериментальным рационами к последнему добавляют расчетное количество крахмала.
В каждой группе животные разделяются не менее чем на две подгруппы:
Получающие ежедневно 40 % раствор этанола через металлический желудочный зонд (из расчета 7,0 г/кг веса) .
Получающие эквиобъемное количество дистиллированной воды.
Введение раствора этанола и дистиллированной воды производится ежедневно в утренние часы до кормления.
Для изучения алкогольобусловленной патологии у крыс продолжительность эксперимента составляет от 4 до 6 недель.
Оценка степени тяжести токсического воздействия
Для адекватной оценки токсического действия химических веществ необходимо регулярное наблюдение за животными, во время которого отмечаются потребление корма и воды, изменение внешних признаков (волосяного покрова, видимых слизистых), особенности поведения. Не реже 1 раза в неделю для изучения динамики изменений производится взвешивание, исследуется функциональное состояние внутренних органов и систем, биохимические и морфологические изменения крови. Методы для оценки состояния органов и систем выбираются с учетом целей эксперимента, однако они должны быть современными и достаточно чувствительными. При проведении исследования необходимо стремиться к использованию максимально полного набора физиологических, патоморфологических, гематологических и биохимических тестов, как для интегральной оценки состояния, так и для определения степени нарушения отдельных органов и систем.
Степень выраженности патологических изменений, регистрируемых у животных, подвергающихся длительной алкогольной интоксикации на фоне алиментарного дисбаланса, определяется с помощью анализа интегральных, биохимических, гематологических и оценки патоморфологической картины. Для проведения функциональной диагностики состояния внутренних органов используются инструментальные методы – ЭЭГ, ЭКГ.
Интегральные показатели:
*изменение внешних признаков – производится 1 раз в 3 суток, перед очередным введением этанола или дистиллированной воды, путем бальной оценки изменения окраса шерсти и волосяного покрова по следующей схеме (таблица 4):
|
Таблица 4 Шкала изменений внешних признаков крыс |
||
|
Баллы или символы |
Описание изменения |
|
|
Выпадение шерсти |
||
|
Загрязненный |
||
|
Не загрязненный |
||
*изменение степени активности - оценивается в баллах 1 раз в 3 суток до этанольной затравки или водной нагрузки по следующей схеме (таблица 5)
*изменение массы тела животных - регистрируется путем взвешивания через каждые 7 суток эксперимента до закладки корма и этанольной затравки
*объем суточного потребления пищи и воды; экскреция веществ.
Шкала изменения активности крыс в токсикологическом эксперименте
|
Баллы, символы /+/ |
Степень активности |
Описание активности |
|
|
|
Погибшее животное |
|
|
Кома (отсутствие активности) |
Боковое положение; обездвиженность; отсутствие активных движений; мышцы расслаблены; дыхание прерывисто; реакции на болевые и тактильные раздражители, в том числе и голосовые, практически отсутствуют. |
|
|
Слабая (минимальная) |
В основном – боковое положение; непроизвольные слабые активные движения; мышцы расслаблены; вялая реакция на болевые и тактильные раздражители, голосовая – слабая. |
|
|
Пассивная |
Животное заторможено, активно по клетке не передвигается, но при подталкивании перемещается на несколько шагов. Положение естественное – на четырех лапах; ощущается тонус мышц. «Избегательная» защитная реакция на раздражители, голосовая реакция слабая. |
|
|
Замедленная (субнормальная) |
Положение – на четырех лапах, медленные активные движения – повороты туловища и небольшие передвижения по клетке, редкие глотательные движения. Реакция на болевые и тактильные раздражители – голосовая и «избегательно-оборонительная» с попытками укусов. При фиксировании рукой за кожу в области спины - изворачивается с «уходом» от экспериментатора. |
|
|
Нормальная |
Интактная крыса. Подвижна; активные движения - перемещение и «изыскание лучшего места в группе»; «настороженно-ожидательная» поза при незначительных болевых и тактильных раздражителях с избеганием, резкой голосовой и активно-оборонительными реакциями, царапающими и кусательными движениями. Хороший аппетит; частые «моющие» движения лапками. |
Биохимические и гематологические показатели.
Исследуются изменения основных биохимических показателей крови и совокупности гематологических параметров, подвергающихся наибольшему влиянию хронической алкогольной интоксикации (таблица 6).
|
Таблица 6 Биохимические и гематологические показатели крыс в токсикологическом эксперименте |
|
|
Объект исследования |
Исследуемые показатели |
|
Сыворотка крови |
аспартатаминотрансфераза, аланинаминотрансфераза, креатининфосфокиназа, гамма-глутамилтрансфераза общий белок, белковые фракции креатинин мочевина |
|
Форменные элементы крови |
количество эритроцитов гематокритная величина цветной показатель количество ретикулоцитов средняя продолжительность жизни эритроцитов лейкоцитарная формула |
Подготовка гистологического материала.
Гистологическому исследованию подвергаются основные «органы – мишени» хронической алкогольной интоксикации – сердце, печень, почки, головной мозг. Необходимо помнить, что качество анализа во многом зависит от подготовки материала, в частности, фиксации исследуемых объектов. Рекомендуется использование для фиксации 10 % раствора формалина или раствор Буэна. При этом предпочтение отдается раствору Буэна, поскольку в данном случае значительно лучше выявляются изменения микроструктуры органов, свойственные длительной алкогольной интоксикации, а именно:
1) в печени – четче прослеживается структурированность цитоплазмы (вакуолизация, «булыжность» - неоднородность прокрашивания цитоплазмы клеток внутри долек), особенности изменения кровенаполнения центральных вен гемокапилляров;
2) в почках – в морфологии эпителиальной выстилки канальцев отчетливее отражаются неоднородности цитоплазматических структур с особенно частым поражением апикальных частей;
3) в легких – в соединительно-тканных межальвеолярных перегородках значительно резче выявляются гипертрофированные, со светлой цитоплазмой клетки, часть которых становится полиплоидными. Чаще отмечаются изменения со стороны альвеолярного эпителия, клетки которого слущиваются в просвет альвеол;
4) в селезенке – лучше проявляется структура ретикулярных клеток, синусов красной пульпы, где отмечается большее разрушение эритроцитов.
Таким образом, применение модели алкогольобусловленной патологии на фоне алиментарного дисбаланса предполагает изучение в экспериментальных условиях наиболее широкого круга изменений внутренних органов и систем, сравнимых с таковыми у человека при злоупотреблении алкоголем. Система оценки основных интегральных, биохимических, гематологических показателей и особенностей патоморфологической картины позволяет на протяжении всего периода исследования контролировать характер и степень патологических изменений.
ЛИТЕРАТУРА
1. Берзиня Н.И. Птицы в эксперименте // Лабораторные животные. – 1995. – V. - №2. – С.99-113.
2. Регламентация экспериментов на животных – этика, законодательства, альтернативы. / Под ред. Н. А. Горбуновой. – М., 1998.
5. Мяленкова И.Ю. Лабораторная собака // Лабораторные животные. – 1994. – IV. - №4. – С.234-246
6. Нужный В.П. Методологические аспекты оценки токсичности спиртосодержащих жидкостей и алкогольных напитков // Токсикологический вестник. – 1999. - №4. – С2-10.
7. Островский Ю.М. Экспериментальная витаминология. – Минск, 1979. – 450с.
8. Покровский А.А. с соавт., О соотношении между содержанием свободных аминокислот в тканях и плазме крови при белковой недостаточности в эксперимента // Вопросы питания – 1974. - №1. – С.8-15.
9. Требования Международного комитета по науке по использованию в экспериментальных исследованиях лабораторных животных // Бюллетень ИКЛАС. – 1978. - № 24. – С. 4-5.
10. Штефель В.О. О сроках воздействия при моделировании интоксикаций в токсиколого-гигиенических исследования // Гигиена и санитария. – 1996. - №8. – С.70-72.
11. Sos J et al., Diets for animals experiments. – Budapest,1974.